题目内容
9.纳米TiO2作为一种光催化剂越来越受到人们的关注,现正广泛开发运用.(1)制取纳米TiO2的方法很多,氢氧火焰水解法是将TiCl4气体导入氢氧火焰中(700~1000℃)进行水解,其化学反应式为:TiCl4+2H2O$\frac{\underline{\;高温\;}}{\;}$TiO2+4HCl.
(2)纳米二氧化钛可光解挥发性有机污染物(VOCs),若无水蒸气存在,三氯乙烯降解反应为:C2HCl3+2O2→2CO2+HCl+Cl2,若有足够量的降解后的尾气,实验室检验产物中有氯气的简单方法是:用湿润的KI-淀粉试纸检验;通过质谱仪发现还有多种副反物,其中之一为:
 ,则该有机物核磁共振氢谱有3个峰.
,则该有机物核磁共振氢谱有3个峰.(3)利用半导材料TiO2与染料、铂电极及I${\;}_{3}^{-}$和I-的混合物作电解质(I2+I-?I${\;}_{3}^{-}$),可构成染料敏化太阳能电池(DSSCs)工作原理如图1,该电池工作时,正极的电极反应为:I3-+2e-=3I-.
(4)在不同的载体(钛片、铝片、陶瓷)表面制备二氧化钛薄膜,来考察不同载体TiO2薄膜光催化使甲基橙脱色,每次光照20min取一次样,实验结果如图2.
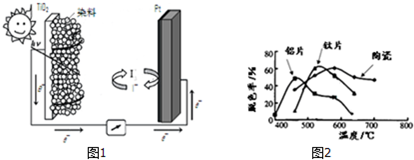
下列说法正确的是bd.
(a)不同载体,无论何种温度一定是钛片最好
(b)约在520℃时,钛片载体的光催化活性最好
(c)无论何种载体,催化活性总是随温度的升高而升高
(d)不同负载TiO2薄膜的光催化活性不同.
分析 (1)TiCl4水解生成二氧化钛和氯化氢;
(2)氯气具有强氧化性,可与KI反应生成碘单质,淀粉遇碘变蓝色;分子中有几种氢,核磁共振氢谱有几种峰;
(3)由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原;
(4)根据图中脱色率与温度关系解题.
解答 解:(1)高温条件下,TiCl4水解生成二氧化钛和氯化氢,化学反应式为TiCl4+2H2O$\frac{\underline{\;高温\;}}{\;}$TiO2+4HCl,
故答案为:TiCl4+2H2O$\frac{\underline{\;高温\;}}{\;}$TiO2+4HCl;
(2)氯气具有强氧化性,可与KI反应生成碘单质,淀粉遇碘变蓝色,所以可将湿润的淀粉KI试纸置于集气瓶口,证明有氯气;分子中有3种氢,核磁共振氢谱有3个峰,
故答案为:用湿润的KI-淀粉试纸检验;3;
(3)由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原,正极反应为I3-+2e-=3I-,
故答案为:I3-+2e-=3I-;
(4)a.由图知,500度以下钛片最差,故a错误;
b.由图知,在520℃时,脱色率最高,钛片载体的光催化活性最好,故b正确;
c.520℃后钛片催化活性随温度的升高而较低,故c错误;
d.由图知,相同温度时,不同的载体(钛片、铝片、陶瓷),TiO2薄膜的光催化活性不同,故d正确.
故答案为:bd.
点评 本题考查原电池的工作原理、物质的检验、元素化合物的性质等,题目难度不大,本题注意把握电极反应式的书写,图中电子的移动方向是解答的关键,侧重于考查学生对基础知识的综合应用能力.

| A. | 将40gNaOH溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成1L溶液 | |
| C. | 将1L10mol/L的浓盐酸与9L水混合 | |
| D. | 将10gNaOH溶解于水中配成250mL溶液 |
| A. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | B. | 金刚石和石墨 | ||
| C. | 乙烷和丙烷 | D. | T2O和D2O |
| A. | NaOH | B. | Na2O | C. | H2SO4 | D. | O2 |
| A. | 石墨制成金刚石 | B. | 煤加氢变成人造石油 | ||
| C. | 水变成汽油 | D. | 海水淡化可以缓解淡水危机 |
| A. | NaOH溶液与盐酸中和 | B. | 分解氯酸钾制氧气 | ||
| C. | Zn与CuSO4 溶液的反应 | D. | MgCl2溶液与KOH溶液产生沉淀 |
| A. | =7 | B. | >7 | C. | <7 | D. | 无法确定 |
| A. | 10℃时,块状锌与3 mol/L硫酸溶液反应 | |
| B. | 30℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| C. | 10℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| D. | 30℃时,块状锌与3 mol/L硫酸溶液反应 |
| A. | 高锰酸钾 | B. | 氯化铵和熟石灰 | C. | 碳和浓硫酸 | D. | H2O2和二氧化锰 |