题目内容
19.下列化学反应中,属于氧化还原反应( )| A. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | NH3+HCl═NH4Cl | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | H2SO4+2NaOH═Na2SO4+2H2O |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O反应中存在化合价变化,属于氧化还原反应,故A正确;
B.NH3+HCl═NH4Cl无元素化合价的变化,属于非氧化还原反应,故B错误;
C.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑为分解反应,不存在化合价变化,属于非氧化还原反应,故C错误;
D.H2SO4+2NaOH═Na2SO4+2H2O为复分解反应,不存在化合价变化,不属于氧化还原反应,故D错误;
故选A.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
9.15LNO2通过水后(未完全反应)收集到7L气体(同温同压),则被氧化的NO2有( )
| A. | 4L | B. | 6L | C. | 8L | D. | 12L |
10.下列离子化合物中,阳离子、阴离子半径之比最小的是( )
| A. | NaCl | B. | MgCl2 | C. | KBr | D. | MgBr2 |
14.下列解释事实的化学(或离子)方程式正确的是( )
| A. | 向100ml浓度均为1mol/LFeI2、FeBr2混合溶液中通入标况下4.48L的氯气:3Cl2+2Fe2++4I-=2I2+2Fe3++6Cl- | |
| B. | 将1 mol•L-1 NaAlO2溶液和1.5 mol•L-1的HC1溶液等体积混合:6AlO2-+9H++3H2O═5Al(OH)3↓+Al3+ | |
| C. | 在澄清石灰水中加入过量的Ca(HCO3)2溶液:2OH-+Ca2++2HCO3-═CaCO3↓+CO32-+2H2O | |
| D. | 向NaClO溶液加入少量FeCl2溶液:2Fe2++ClO-+2H+═2Fe3++2H2O+Cl- |
4.根据氧化还原反应及其规律,下列判断正确的是( )
| A. | 2FeCl2+Cl2═2FeCl3,反应中氧化产物和还原产物质量比为1:1 | |
| B. | 根据反应I2+SO2+2H2O═H2SO4+2HI,说明还原性SO2<HI | |
| C. | 8NH3+3Cl2═6NH4Cl+N2中氧化剂和还原剂物质的量之比为3:8 | |
| D. | KClO3+6HCl═3Cl2+KCl+3H2O,每生成3molCl2,转移电子6mol |
8.常温下,200mL0.5mol/L硫酸溶液的pH是( )
| A. | 0 | B. | 1 | C. | 2 | D. | 0.1 |
4.设NA为阿伏伽德罗常数的值.下列有关叙述不正确的是( )
| A. | 44g乙醛与乙酸乙酯的混合物中含氧原子数为NA | |
| B. | 40gH2${\;}_{\;}^{18}$O与40gD2O所含的中子数均为20NA | |
| C. | 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2NA | |
| D. | 62gNa2O与78gNa2O2所含的阴离子数均为NA |

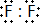 ,两者气态氢化物的稳定性是:HF>HCl(填写化学式).
,两者气态氢化物的稳定性是:HF>HCl(填写化学式).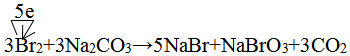 .
.