题目内容
9.15LNO2通过水后(未完全反应)收集到7L气体(同温同压),则被氧化的NO2有( )| A. | 4L | B. | 6L | C. | 8L | D. | 12L |
分析 NO2通入水后发生反应为3NO2+H2O=2HNO3+NO,导致气体体积减小,计算出体积变化量,根据体积差量法计算NO2的体积,再根据二氧化氮与水的反应方程式判断被氧化的二氧化氮的体积.
解答 解:反应后体积减小为15L-7L=8L,则:
3NO2+H2O=2HNO3+NO 体积减小△V
3 2
V(NO2) 8L
解得:V(NO2)=$\frac{8L×3}{2}$=12L,
根据反应3NO2+H2O=2HNO3+NO可知,二氧化氮被氧化生成硝酸,参加反应的二氧化氮中被氧化的占参加反应的二氧化氮的 $\frac{2}{3}$,
则被氧化的二氧化氮的体积为12L×$\frac{2}{3}$=8L,
故选C.
点评 本题考查化学方程式的计算,题目难度中等,明确反应原理及差量法的应用为解答关键,注意掌握氧化还原反应中反应类型的判断方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
10.化学在生产和日常生活中有着重要作用,下列有关说法不正确的是( )
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| D. | 利用粮食酿酒经过了淀粉→葡糖糖→乙醇的化学变化过程 |
17.某校化学课题组探究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺,他们设计的流程如图所示,在“焙烧“过程中铁元素转 为 Fe3O4.下列推断正确的是( )
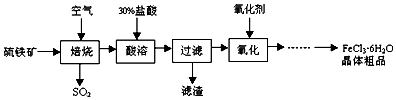

| A. | “焙烧”反应中,氧化产物是SO2,还原产物是Fe3O4 | |
| B. | “酸溶”时的酸可以用稀硫酸代替 | |
| C. | “过滤“后的滤液中Fe3+和Fe2+的浓度比为2:1 | |
| D. | “氧化”时的氧化剂只能选取Cl2 |
4.下列物质在常温下可用铝或铁的容器贮存的是( )
| A. | 浓硫酸 | B. | 稀硝酸 | C. | 王水 | D. | 硫酸铜 |
14.下列物质类型中,前者包括后者的是( )
| A. | 溶液、分散系 | B. | 氧化物、化合物 | C. | 溶液、胶体 | D. | 化合物、电解质 |
1.现有下列八种物质:①H2 ②铝 ③Na2O ④SO2 ⑤HNO3 ⑥KNO3⑦(NH4)2SO4⑧NaCl溶液
(1)按物质的分类方法填写表格的空白处:
(2)写出(NH4)2SO4在水中的电离方程式:(NH4)2SO4═2NH4++SO42-.
(1)按物质的分类方法填写表格的空白处:
| 分类标准 | 金属单质 | 碱性氧化物 | 硝酸盐 | 非电解质 |
| 属于该类的物质(填序号) | ② | ③ | ⑥ | ④ |
18.含有a mol FeBr2的溶液中,通入x mol Cl2.下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( )
| A. | x=0.3a,2Fe2++Cl2→2Fe3++2Cl- | |
| B. | x=0.7a,2Br-+Cl2→Br2+2Cl- | |
| C. | x=1.2a,2Fe2++2Br-+2Cl2→Br2+2Fe3++4Cl- | |
| D. | x=1.5a,2Fe2++4Br-+3Cl2→2Br2+2Fe3++6Cl- |
19.下列化学反应中,属于氧化还原反应( )
| A. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | NH3+HCl═NH4Cl | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | H2SO4+2NaOH═Na2SO4+2H2O |