题目内容
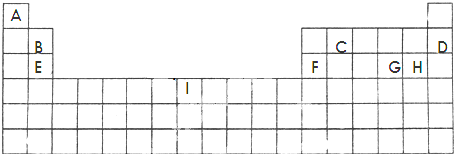
下列各组物质的性质比较中不正确的是( )
| A、氧化性:F2>C12>Br2 |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、热稳定性:SiH4>PH3>H2S |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,单质的氧化性越强,;
B.元素的非金属性越强,最高氧化物对应水化物的酸性越强;
C.元素的金属性越强,最高氧化物对应水化物的碱性越强;
D.元素的非金属性越强,对应的氢化物越稳定.
B.元素的非金属性越强,最高氧化物对应水化物的酸性越强;
C.元素的金属性越强,最高氧化物对应水化物的碱性越强;
D.元素的非金属性越强,对应的氢化物越稳定.
解答:
解:A.非金属性:F>Cl>Br,元素的非金属性越强,单质的氧化性越强,故氧化性:F2>C12>Br2,故A正确;
B.非金属性:Cl>S>P,元素的非金属性越强,最高氧化物对应水化物的酸性越强,故酸性:HClO4>H2SO4>H3PO4,故B正确;
C.金属性:Na>Mg>Al,元素的金属性越强,最高氧化物对应水化物的碱性越强,故碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.非金属性:S>P>Si,元素的非金属性越强,对应的氢化物越稳定,故热稳定性:H2S>PH3>SiH4,故D错误;
故选D.
B.非金属性:Cl>S>P,元素的非金属性越强,最高氧化物对应水化物的酸性越强,故酸性:HClO4>H2SO4>H3PO4,故B正确;
C.金属性:Na>Mg>Al,元素的金属性越强,最高氧化物对应水化物的碱性越强,故碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.非金属性:S>P>Si,元素的非金属性越强,对应的氢化物越稳定,故热稳定性:H2S>PH3>SiH4,故D错误;
故选D.
点评:本题考查元素周期表与元素周期律的综合应用,难度不大.要注意把握元素周期律的递变规律和基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴阳极,槽中盛放含铬废水,原理示意图如图,下列说法正确的是( )
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴阳极,槽中盛放含铬废水,原理示意图如图,下列说法正确的是( )| A、A电源的负极 |
| B、阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
| C、阴极区附近溶液的pH降低 |
| D、若不考虑气体的溶解,当收集到H213.44L时有0.1molCr2O72-被还原 |
在体积相同的三个容器里分别充入三种气体①氢气;②二氧化碳;③氧气,并保持三个容器内气体的温度和密度均相等,下列说法正确的是( )
| A、分子数目:①=②=③ |
| B、质量关系:①<③<② |
| C、压强关系:①>③>② |
| D、原子数目:②>③>① |
NA为阿伏加德罗常数,下列有关说法中不正确的是( )
| A、标准状况下,22.4 L氦气含有NA个氦原子 |
| B、20 g重水含有10 NA个电子 |
| C、12.5 mL l6 mol?L-1浓硫酸与足量铜反应,转移电子数为0.2 NA |
| D、1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1 NA |
下列用来表示物质变化的方程式正确的是( )
| A、NaHS溶液的水解方程式:HS-+H2O?H3O++S2- | ||||
B、以金属Pt为阳极电解硫酸铜溶液:2Cu2++2H2O
| ||||
C、硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH-
| ||||
| D、强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+H+ |