题目内容
根据已学知识,请你回答下列问题:
(1)试比较含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3 HClO4.
(2)根据价层电子对互斥理论判断:H2O的VSEPR构型为 H3O+的分子立体结构为 .
(3)沸点比较:邻羟基苯甲醛 对羟基苯甲醛(填“>”、“<”或“=”)
(4)在下列物质①NH3、②BF3、③HCl、④SO3,属于非极性分子的是(填番号) .
(5)①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有 (填序号).
(6)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为 .
(7)配离子[TiCl(H2O)5]2+的中心离子的符号为 ,配位数为 .
(1)试比较含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3
(2)根据价层电子对互斥理论判断:H2O的VSEPR构型为
(3)沸点比较:邻羟基苯甲醛
(4)在下列物质①NH3、②BF3、③HCl、④SO3,属于非极性分子的是(填番号)
(5)①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(6)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为
(7)配离子[TiCl(H2O)5]2+的中心离子的符号为
考点:判断简单分子或离子的构型,配合物的成键情况,分子晶体,极性分子和非极性分子,原子轨道杂化方式及杂化类型判断,氢键的存在对物质性质的影响
专题:
分析:(1)判断含氧酸(含有氧元素的酸)酸性强弱的一条经验规律是:含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强;
(2)根据价层电子对互斥理论确定其空间构型,价层电子对个数=σ键个数+孤电子对个数,据此分析解答;
(3)根据氢键对物理性质的影响分析;
(4)对于ABn型分子,A原子的最外层电子,若完全成键,属于非极性分子,若不完全成键,则属于极性分子,据此分析;
(5)根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数;
(6)根据氯化铁的性质进行判断;
(7)配离子[TiCl(H2O)5]2+中Cl-、H2O含有孤对电子对是配体,根据离子电荷判断中心离子Tin+的电荷.
(2)根据价层电子对互斥理论确定其空间构型,价层电子对个数=σ键个数+孤电子对个数,据此分析解答;
(3)根据氢键对物理性质的影响分析;
(4)对于ABn型分子,A原子的最外层电子,若完全成键,属于非极性分子,若不完全成键,则属于极性分子,据此分析;
(5)根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数;
(6)根据氯化铁的性质进行判断;
(7)配离子[TiCl(H2O)5]2+中Cl-、H2O含有孤对电子对是配体,根据离子电荷判断中心离子Tin+的电荷.
解答:
解:(1)含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强,所以含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越强,酸性由强到弱:HClO3<HClO4,故答案为:<;
(2)H2O中心原子O原子成2个σ键、含有2对孤对电子,价层电子对个数=σ键个数+孤电子对个数=2+2=4,杂化轨道数为4,采取sp3杂化,H2O的VSEPR构型是正四面体;
H3O+的中心原子O价层电子对个数=3+
=4,采取sp3杂化,有一对孤电子对,分子构型为三角锥型,故答案为:正四面体;
(3)邻羟基苯甲醛能形成分子内氢键,对羟基苯甲醛能形成分子间氢键,所以邻羟基苯甲醛的熔点低于对羟基苯甲醛,故答案为:<;
(4):①NH3中元素化合价为-3,N原子最外层5个电子未全部成键,为极性分子;
②BF3中B元素化合价为+3,B原子最外层3个电子全部成键,为非极性分子;
③HCl中Cl元素化合价为+1,Cl原子最外层7个电子全部成键,为极性分子;
④SO3中S元素化合价为+6,S原子最外层6个电子全部成键,为非极性分子;
故答案为:②④;
(5)①苯中碳原子成1个C-Hδ键,2个C-Cδ键,同时参与成大π键,杂化轨道数为1+2=3,所以碳原子采取sp2杂化;
②CH3OH分子中中心原子C价电子对数=4+
=4,采取sp3杂化;
③HCHO分子中中心原子C价电子对数=3+
=3,采取sp2杂化;
④CS2分子中中心原子C价电子对数=2+
=2,采取sp杂化;
⑤CCl4分子中中心原子C价电子对数=4+
=4,采取sp3杂化;
故答案为:①③;
(6)由题目信息可知,氯化铁的熔沸点低,易升华,所以氯化铁为分子晶体,故答案为:分子晶体;
(7)配离子[TiCl(H2O)5]2+的中心离子所带的电荷2+1=3,故中心离子为Ti3+,Cl-、H2O含有孤对电子对是配体,配位数是6,故答案为:Ti3+;6.
(2)H2O中心原子O原子成2个σ键、含有2对孤对电子,价层电子对个数=σ键个数+孤电子对个数=2+2=4,杂化轨道数为4,采取sp3杂化,H2O的VSEPR构型是正四面体;
H3O+的中心原子O价层电子对个数=3+
| 6-1-1×3 |
| 2 |
(3)邻羟基苯甲醛能形成分子内氢键,对羟基苯甲醛能形成分子间氢键,所以邻羟基苯甲醛的熔点低于对羟基苯甲醛,故答案为:<;
(4):①NH3中元素化合价为-3,N原子最外层5个电子未全部成键,为极性分子;
②BF3中B元素化合价为+3,B原子最外层3个电子全部成键,为非极性分子;
③HCl中Cl元素化合价为+1,Cl原子最外层7个电子全部成键,为极性分子;
④SO3中S元素化合价为+6,S原子最外层6个电子全部成键,为非极性分子;
故答案为:②④;
(5)①苯中碳原子成1个C-Hδ键,2个C-Cδ键,同时参与成大π键,杂化轨道数为1+2=3,所以碳原子采取sp2杂化;
②CH3OH分子中中心原子C价电子对数=4+
| 4-4 |
| 2 |
③HCHO分子中中心原子C价电子对数=3+
| 4-1×2-2 |
| 2 |
④CS2分子中中心原子C价电子对数=2+
| 4-2×2 |
| 2 |
⑤CCl4分子中中心原子C价电子对数=4+
| 4-1×4 |
| 2 |
故答案为:①③;
(6)由题目信息可知,氯化铁的熔沸点低,易升华,所以氯化铁为分子晶体,故答案为:分子晶体;
(7)配离子[TiCl(H2O)5]2+的中心离子所带的电荷2+1=3,故中心离子为Ti3+,Cl-、H2O含有孤对电子对是配体,配位数是6,故答案为:Ti3+;6.
点评:本题考查了杂化轨道、氢键、晶体类型的判断等,难度中等,注意基础知识的掌握与规律的总结.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
人类的生活离不开材料,
①塑料广泛应用与生产、生活的各个领域,聚乙烯塑料属于 (填序号)
A.有机高分子材料 B.无机非金属材料 C.金属材料
②蚕丝、尼龙、棉花这三种常见的纤维中,主要成分为蛋白质的是 .
①塑料广泛应用与生产、生活的各个领域,聚乙烯塑料属于
A.有机高分子材料 B.无机非金属材料 C.金属材料
②蚕丝、尼龙、棉花这三种常见的纤维中,主要成分为蛋白质的是
下列各组物质的性质比较中不正确的是( )
| A、氧化性:F2>C12>Br2 |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、热稳定性:SiH4>PH3>H2S |
分类是化学学习和研究的常用手段.下列分类依据和结论都正确的是( )
| A、H2O、HCOOH、(NH4)2Fe(SO4)2均含有氧,都是氧化物 |
| B、HCl、H2SO4、HNO3均具有氧化性,都是氧化性酸 |
| C、赤铁矿、磁铁矿、黄铁矿、孔雀石都是常见的铁矿石 |
| D、Na2CO3、Ba(OH)2、NH4Cl、Na2O2都属于离子化合物 |
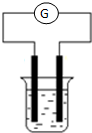 现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下: