题目内容
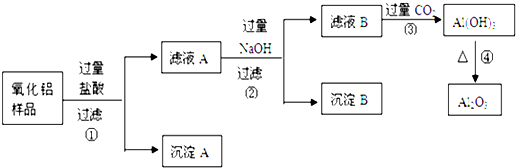
某化学小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下图所示:
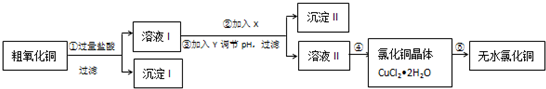
(1)步骤①中氧化铜与盐酸反应的离子方程式是 .
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)、普通漏斗外,还需要使用的玻璃仪器是 .
(3)已知:
参照表中给出的数据和试剂,请回答:
步骤②的目的是 ,反应的离子方程式是 .步骤③中调节溶液pH的范围是 ,试剂Y是 (填化学式).

(1)步骤①中氧化铜与盐酸反应的离子方程式是
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)、普通漏斗外,还需要使用的玻璃仪器是
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的试剂:a.NaOH b.H2O2 c.Na2CO3 d.CuO | ||
步骤②的目的是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:粗CuO中含有FeO和不溶于酸的杂质,将粗CuO溶于过量盐酸,发生的反应有FeO+2HCl=FeCl2+H2O、CuO+2HCl=CuCl2+H2O,然后过滤,得到沉淀I为不溶于酸的杂质,溶液I中溶质为FeCl2、CuCl2和HCl,向溶液I中加入X、Y然后调节pH过滤,得到沉淀II,溶液II,除去FeCl2、CuCl2和HCl中的FeCl2,根据氢氧化物沉淀需要的pH知,应该先将FeCl2氧化为铁盐,为不引进新的杂质,氧化剂X应该为Cl2或H2O2,然后向溶液中加入CuO调节溶液的pH,所以Y可以是CuO,则沉淀II为Fe(OH)3,然后将溶液II蒸发浓缩、冷却结晶得到CuCl2.2H2O,最后在HCl氛围中加热CuCl2.2H2O得到CuCl2;
(1)碱性氧化物和酸反应生成盐和水;
(2)需要引流的仪器和盛放溶液的仪器;
(3)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子;当铁离子完全沉淀时溶液的pH为3.2,当铜离子出现沉淀时溶液的pH为4.7,调节溶液的pH要除去铁离子而不能除去铜离子.
(1)碱性氧化物和酸反应生成盐和水;
(2)需要引流的仪器和盛放溶液的仪器;
(3)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子;当铁离子完全沉淀时溶液的pH为3.2,当铜离子出现沉淀时溶液的pH为4.7,调节溶液的pH要除去铁离子而不能除去铜离子.
解答:
解:粗CuO中含有FeO和不溶于酸的杂质,将粗CuO溶于过量盐酸,发生的反应有FeO+2HCl=FeCl2+H2O、CuO+2HCl=CuCl2+H2O,然后过滤,得到沉淀I为不溶于酸的杂质,溶液I中溶质为FeCl2、CuCl2和HCl,向溶液I中加入X、Y然后调节pH过滤,得到沉淀II,溶液II,除去FeCl2、CuCl2和HCl中的FeCl2,根据氢氧化物沉淀需要的pH知,应该先将FeCl2氧化为铁盐,为不引进新的杂质,氧化剂X应该为Cl2或H2O2,然后向溶液中加入CuO调节溶液的pH,所以Y可以是CuO,则沉淀II为Fe(OH)3,然后将溶液II蒸发浓缩、冷却结晶得到CuCl2.2H2O,最后在HCl氛围中加热CuCl2.2H2O得到CuCl2.
(1)通过以上分析知,CuO和酸反应生成铜盐和水,离子方程式为CuO+2H+=Cu2++H2O,故答案为:CuO+2H+=Cu2++H2O;
(2)还需要起引流作用的玻璃棒,盛放溶液的烧杯,故答案为:玻璃棒、烧杯;
(3)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子,选取双氧水时发生的离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O;当铁离子完全沉淀时溶液的pH为3.2,当铜离子出现沉淀时溶液的pH为4.7,调节溶液的pH要除去铁离子而不能除去铜离子,所以溶液的pH范围为3.2-4.7,可以加入CuO调节溶液的pH,故答案为:将Fe2+氧化成Fe3+;2Fe2++H2O2+2H+=2Fe3++2H2O; 3.2-4.7; CuO.
(1)通过以上分析知,CuO和酸反应生成铜盐和水,离子方程式为CuO+2H+=Cu2++H2O,故答案为:CuO+2H+=Cu2++H2O;
(2)还需要起引流作用的玻璃棒,盛放溶液的烧杯,故答案为:玻璃棒、烧杯;
(3)步骤②加入氧化剂将亚铁离子氧化生成铁离子,然后调节溶液的pH除去铁离子,选取双氧水时发生的离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O;当铁离子完全沉淀时溶液的pH为3.2,当铜离子出现沉淀时溶液的pH为4.7,调节溶液的pH要除去铁离子而不能除去铜离子,所以溶液的pH范围为3.2-4.7,可以加入CuO调节溶液的pH,故答案为:将Fe2+氧化成Fe3+;2Fe2++H2O2+2H+=2Fe3++2H2O; 3.2-4.7; CuO.
点评:本题考查混合物的分离和提纯,涉及除杂剂的选取、氧化还原反应、仪器的选取等知识点,侧重考查整体分析解答能力,会根据仪器的作用选取仪器,难点是确定调节溶液的pH时pH的取值范围,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质的性质比较中不正确的是( )
| A、氧化性:F2>C12>Br2 |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、热稳定性:SiH4>PH3>H2S |
分类是化学学习和研究的常用手段.下列分类依据和结论都正确的是( )
| A、H2O、HCOOH、(NH4)2Fe(SO4)2均含有氧,都是氧化物 |
| B、HCl、H2SO4、HNO3均具有氧化性,都是氧化性酸 |
| C、赤铁矿、磁铁矿、黄铁矿、孔雀石都是常见的铁矿石 |
| D、Na2CO3、Ba(OH)2、NH4Cl、Na2O2都属于离子化合物 |
五倍子是一种常见的中草药,其有效成分为X.在一定条件下X可分别转化为Y、Z.下列说法错误的是( )
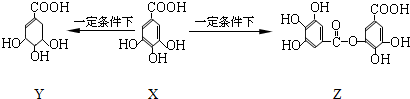

| A、1molX最多能与2molBr2发生取代反应 |
| B、Y分子结构中有2个手性碳原子 |
| C、Y能发生加成、取代、消去、氧化、缩聚反应 |
| D、1mol Z最多能与7molNaOH发生反应 |
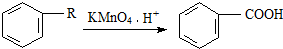
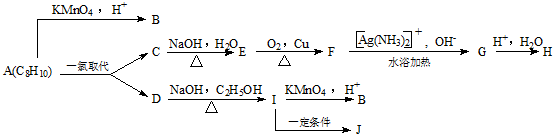
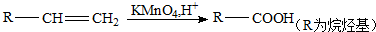 ,芳香烃A的分子式为C8H10,在一定条件下能发生下列转化,B、H属同系物,J是一种常见的高分子塑料.
,芳香烃A的分子式为C8H10,在一定条件下能发生下列转化,B、H属同系物,J是一种常见的高分子塑料.