题目内容
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+则下列说法正确的是( )
| A、该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物 |
| B、充分反应后可以看到白色沉淀和气体生成 |
| C、标准状况下,每生成22.4 L O2,则有4 mol Na2O2被还原 |
| D、若有4 mol Na2O2参加反应,则反应中共转移6NA个电子 |
考点:氧化还原反应
专题:
分析:由4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,可知Fe元素的化合价由+2价升高为+3价,过氧化钠中O元素的化合价由-1价升高为0,由-1价降低为-2价,该反应中转移电子数为6e-,以此来解答.
解答:
解:A.反应中O、Fe元素化合价升高,O2、Fe(OH)3均为氧化产物,Na2O2中O元素化合价为-1价,反应中化合价既升高又降低,Na2O2即为氧化剂也为还原剂,故A错误;
B.反应过程中亚铁离子被氧化为三价铁离子,反应过程中看不到白色沉淀转化为灰绿色再转化为红褐色沉淀的现象,故B错误;
C.由方程式可知,生成22.4 L O2,即1mol,转移6 mol电子,有3mol Na2O2被还原,故C错误;
D.4mol过氧化钠有1mol做还原剂,3mol做氧化剂,每生成1 mol O2反应过程中共转移6 mol电子,故D正确.
故选D.
B.反应过程中亚铁离子被氧化为三价铁离子,反应过程中看不到白色沉淀转化为灰绿色再转化为红褐色沉淀的现象,故B错误;
C.由方程式可知,生成22.4 L O2,即1mol,转移6 mol电子,有3mol Na2O2被还原,故C错误;
D.4mol过氧化钠有1mol做还原剂,3mol做氧化剂,每生成1 mol O2反应过程中共转移6 mol电子,故D正确.
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子数的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
相关题目
 如图表示反应2SO2(g)+O2(g)═2SO3(g)△H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )
如图表示反应2SO2(g)+O2(g)═2SO3(g)△H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )| A、t1时减小了SO2 的浓度,增加了SO3的浓度,平衡向逆反应方向移动 |
| B、t1时降低了温度,平衡向正反应方向移动 |
| C、t1时减小了压强,平衡向逆反应方向移动 |
| D、t1时增加了SO2 和O2的浓度,平衡向正反应方向移动 |
下列关于乙烯的说法错误的是( )
| A、乙烯的结构简式可以表示为CH2CH2 |
| B、收集乙烯可用排空气法 |
| C、可作香蕉等水果的催熟剂 |
| D、燃烧时火焰明亮,同时产生黑烟 |
关于CH4和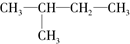 的叙述正确的是( )
的叙述正确的是( )
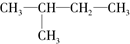 的叙述正确的是( )
的叙述正确的是( )| A、均能用CnH2n+2组成来表示 |
| B、与所有烷烃互为同素异形体 |
| C、因为它们结构相似,所以它们的化学性质相似,但物理性质不相同 |
| D、通常状况下它们都是气态烷烃 |
立方烷(C8H8)的碳架结构如图,则它的五氯代物有( )种
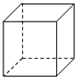

| A、3 | B、4 | C、5 | D、6 |
下列说法不正确的是( )
| A、“白色污染”主要是由合成材料的废弃物,特别是一些塑料制品废弃物造成的 |
| B、“白色污染”只能影响环境卫生,没有其他危害 |
| C、治理“白色污染”主要应从减少使用、加强回收和再利用开始 |
| D、使用可降解塑料是治理“白色污染”的理想方法 |
下表为4种常见溶液中溶质的质量分数和物质的量浓度:这4种溶液中密度最小的是( )
| 溶 质 | HCl | NaOH | CH3COOH | HNO3 |
| 溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
| 物质的量浓度/mol L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
| A、HCl |
| B、NaOH |
| C、CH3COOH |
| D、NO3 |
假如12C相对原子质量为24,以0.024千克12C所含12C的原子数为阿伏加德罗常数.下列数值肯定不变的是( )
| A、阿伏加德罗常数 |
| B、摩尔质量 |
| C、一定质量气体的体积 |
| D、O2的相对分子质量 |
