题目内容
在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)?2HI(g)△H<0反应中各物质的浓度随时间变化情况如图1:

(1)该反应的化学平衡常数表达式为 .
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写“增大”、“减小”或“不变”)HI浓度的变化正确的是 (用图2中a-c的编号回答)
②若加入I2,H2浓度的变化正确的是 ,(用图2中d-f的编号回答)
(3)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况.

(1)该反应的化学平衡常数表达式为
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K
②若加入I2,H2浓度的变化正确的是
(3)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况.
考点:化学平衡的计算
专题:
分析:(1)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算;
(2)①根据化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,生成物浓度增大,反之,若平衡逆向移动,化学平衡常数K减少,生成物浓度减少;
②若加入I2,平衡正向移动,H2浓度减少;
(3)反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小.
(2)①根据化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,生成物浓度增大,反之,若平衡逆向移动,化学平衡常数K减少,生成物浓度减少;
②若加入I2,平衡正向移动,H2浓度减少;
(3)反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小.
解答:
解:(1)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K=
,故答案为:K=
;
(2)①该反应放热,升高温度,平衡逆向移动,化学平衡常数K减小,生成物浓度减少,故答案为:减小;c;
②若加入I2,平衡正向移动,H2浓度减少,故答案为:e;
(3)H2(g)+I2(g)?2HI(g),反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小,碘化氢浓度减小一半为0.25mol/L,画出的变化图象如图: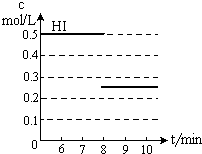 ,故答案为:
,故答案为: .
.
| c2(HI) |
| c(H2)?c(I2) |
| c2(HI) |
| c(H2)?c(I2) |
(2)①该反应放热,升高温度,平衡逆向移动,化学平衡常数K减小,生成物浓度减少,故答案为:减小;c;
②若加入I2,平衡正向移动,H2浓度减少,故答案为:e;
(3)H2(g)+I2(g)?2HI(g),反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小,碘化氢浓度减小一半为0.25mol/L,画出的变化图象如图:
 ,故答案为:
,故答案为: .
.
点评:本题主要考查了平衡常数、化学平衡移动以及化学反应速率的计算,难度不大,需要注意的是:化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,反之则减少.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列实验操作中,正确的是( )
| A、蒸发结晶时,应将溶液蒸干后才停止加热 |
| B、蒸馏中,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
| D、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释至刻度线 |
既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
| A、混合气通过盛有水的洗气瓶 |
| B、通过装有过量溴水的洗气瓶 |
| C、混合气与足量溴蒸气混合 |
| D、混合气与过量氢气混合 |
下列化合物的一氯代物的数目排列顺序正确的是( )
①CH3CH2CH2CH2CH2CH3②(CH3)2CHCH(CH3)2③(CH3)3CCH2CH3 ④(CH3)3CC(CH3)3.
①CH3CH2CH2CH2CH2CH3②(CH3)2CHCH(CH3)2③(CH3)3CCH2CH3 ④(CH3)3CC(CH3)3.
| A、①>②>③>④ |
| B、③=①>②>④ |
| C、③>②>④>① |
| D、②>③=①>④ |
要配制浓度为2mol?L-1NaOH溶液100mL,下面的操作正确的是( )
| A、称取8gNaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B、称取8gNaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL |
| C、称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀. |
| D、用100mL量筒量取40mL5mol?L-1NaOH溶液,倒入烧杯中,加水搅拌,将溶液转移至100mL容量瓶中,洗涤烧杯和玻璃棒并转移洗涤液,再加水至刻度,摇匀. |
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+则下列说法正确的是( )
| A、该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物 |
| B、充分反应后可以看到白色沉淀和气体生成 |
| C、标准状况下,每生成22.4 L O2,则有4 mol Na2O2被还原 |
| D、若有4 mol Na2O2参加反应,则反应中共转移6NA个电子 |

