题目内容
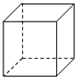
立方烷(C8H8)的碳架结构如图,则它的五氯代物有( )种

| A、3 | B、4 | C、5 | D、6 |
考点:有机化合物的异构现象,常见有机化合物的结构
专题:有机化学基础
分析:采用换元法,将氯原子代替氢原子,氢原子代替氯原子,从立方烷(C8H8)的三氯代物种类,即为立方烷的五氯代物的种类.
解答:
解:立方烷(C8H8)的三氯代物:固定立方烷中相邻的两个顶点,则第三个点的位置可以是与任意两个固定顶点相邻的一个顶点、与两个顶点所在面上的面对角线的顶点,与任意两个固定顶点的体对角线的顶点,因此:立方烷(C8H8)的三氯代物为3种,所以立方烷的五氯代物有3种,
故选:A.
故选:A.
点评:本题考查同分异构体的书写,难度不大,注意体会利用采用换元法确定立方烷的五氯代物的种类.

练习册系列答案
相关题目
下列化合物的一氯代物的数目排列顺序正确的是( )
①CH3CH2CH2CH2CH2CH3②(CH3)2CHCH(CH3)2③(CH3)3CCH2CH3 ④(CH3)3CC(CH3)3.
①CH3CH2CH2CH2CH2CH3②(CH3)2CHCH(CH3)2③(CH3)3CCH2CH3 ④(CH3)3CC(CH3)3.
| A、①>②>③>④ |
| B、③=①>②>④ |
| C、③>②>④>① |
| D、②>③=①>④ |
在密闭容器中,反应:CH4(g)+H2O(g)?CO(g)+H2(g)△H>0,达到平衡,下列叙述不正确的是( )
| A、增加甲烷的量,△H增大 |
| B、增加水蒸气的量,可提高甲烷的转化率 |
| C、升高温度,逆反应速率增大 |
| D、增大体系压强,该反应的化学平衡常数不变 |
下列关于热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2反应的中和热△H=-114.6kJ?mol-1 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0 kJ?mol-1 |
| C、需要加热才能发生的反应一定是吸热反应 |
| D、若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+则下列说法正确的是( )
| A、该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物 |
| B、充分反应后可以看到白色沉淀和气体生成 |
| C、标准状况下,每生成22.4 L O2,则有4 mol Na2O2被还原 |
| D、若有4 mol Na2O2参加反应,则反应中共转移6NA个电子 |
检验某未知溶液是否含有SO42-离子,你认为合理的方法是( )
| A、先加HNO3再加稀BaCl2溶液 |
| B、先加稀盐酸,再加入BaCl2溶液 |
| C、加入BaCl2溶液 |
| D、加入Ba(NO3)2溶液 |
某主族元素的原子最外层电子排布是5s1,下列描述中正确的是( )
| A、其单质常温下跟水反应不如钠剧烈 |
| B、其原子半径比钾原子半径小 |
| C、其碳酸盐易溶于水 |
| D、其氢氧化物不能使氢氧化铝溶解 |
已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则下列说法正确的是( )
| A、浓硫酸和稀NaOH溶液反应,生成 l mol水时放热57.3 kJ |
| B、含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C、1L 0.l mol/L CH3COOH与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ |
| D、1L 0.l mol/L HNO3与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、24 g氢化钠(NaH)固体中阴离子所含电子总数为2NA |
| B、1 mol/L FeCl3溶液中Fe3+的数目小于NA |
| C、在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA |
| D、标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA |