题目内容
14.实验室需用到900mL0.1mol/L的稀盐酸,拟用量筒取用9mol/L的浓盐酸在容量瓶中进行配制.下列有关说法正确的是( )| A. | 应量取的浓盐酸的体积是10.0mL | |
| B. | 若开始时洁净的容量瓶中有少许蒸馏水,对实验没有影响 | |
| C. | 量取浓盐酸时,因浓盐酸有挥发性,所以要多量取lmL浓盐酸 | |
| D. | 定容摇匀后,发现液面低于刻度线,应立即加少量蒸馏水补至刻度线 |
分析 A.依据溶液稀释前后所含溶质的物质的量不变计算,应该配制1000mL盐酸;
B.定容时需要加蒸馏水;
C.盐酸挥发的量很少,而且不能确定;
D.定容摇匀后,发现液面低于刻度线,加少量蒸馏水补齐,导致溶液的体积偏大.
解答 解:A.需用到900mL0.1mol/L的稀盐酸,要用1000ml容量瓶配制,设需要浓盐酸的体积为V,则V×9mol/L=0.1mol/L×1L,解得V=0.0111L=11.1mL,故A错误;
B.定容时应继续加人蒸馏水,所以开始时洁净的容量瓶中有少许蒸馏水,对实验没有影响,故B正确;
C.盐酸挥发的量很少,而且不能确定,所以不能随意更改盐酸的体积,故C错误;
D.定容摇匀后,发现液面低于刻度线,加少量蒸馏水补齐,导致溶液的体积偏大,溶液浓度偏小,故D错误;
故选:B.
点评 本题考查了配制一定物质的量浓度溶液,明确配制原理是解题关键,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
11.下列说法中正确的是( )
| A. | CuCl2溶液蒸干灼烧后得到CuCl2固体 | |
| B. | 火力发电的目的是使化学能转换为电能 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性. | |
| D. | 将FeCl3固体溶于适量蒸馏水来配制FeCl3溶液 |
2.铜钱在历史上曾经是一种广泛流通的货币.从物理性质和化学性质的角度分析,铜常用于制造货币的说法正确的是( )
| A. | 铜来源广泛,易于从自然界冶炼得到 | |
| B. | 铜的化学性质比较稳定,不易被腐蚀,铜的熔点比较低,容易冶炼铸造成型 | |
| C. | 铜的外观为紫红色,大方美观,易于被人们接受 | |
| D. | 铜的化学性质不稳定,在空气中易转化为铜绿,铜绿具有抗腐蚀能力,易于流通 |
9.实验室中需要配制2mol/L的NaCl溶液450mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是( )
| A. | 450mL,52.65g | B. | 500mL,58.5g | C. | 450mL,117g | D. | 500mL,52.3g |
19.已知某饱和溶液的①溶液质量,②溶剂质量,③溶液体积,④溶质的摩尔质量,⑤溶质的溶解度,⑥溶液的密度.利用以上部分已知条件不能计算出该饱和溶液的物质的量的浓度的是( )
| A. | ①②④⑥ | B. | ②④⑤ | C. | ①②③④ | D. | ④⑤⑥ |
6.Na2S2O3•5H2O(俗称海波)是照相业常用的一种定影剂,常采用下法制备:将亚硫酸钠溶液与硫粉混合共热,生成硫代硫酸钠Na2SO3+S$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3,滤去硫粉,再将滤液浓缩、冷却,即有Na2S2O3•5H2O晶体析出.该法制得的晶体中常混有少量Na2SO3和Na2SO4的杂质.为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的H2SO4溶液20mL,充分反应后滤出硫,并将滤液微热(假定生成的SO2全部逸出),测得有关实验数据如下(标准状况):
(1)样品与硫酸可能发生反应的离子方程式为S2O32-+2H+=S↓+SO2↑+H2O、SO32-+2H+=SO2↑+H2O.
(2)根据上表数据分析,该样品A(填选项字母)
A.含有Na2S2O3、Na2SO3和Na2SO4三种成分
B.含有Na2S2O3和Na2SO3两种成分
C.只含有Na2S2O3
(3)求第三份样品中各成分的物质的量.
(4)求所加硫酸的物质的量浓度.
(5)若将63g该样品与一定量的该硫酸溶液微热,回答问题:
①欲计算生成SO2的体积,还需要提供的一个数据是(用a表示该数值,并注明单位)硫酸溶液的体积.当a=0.06时,V(SO2)=5.6;
②(2分)在图1上画出b随a变化的曲线
(6)图2是实验室制取SO2并验证SO2的某些性质的装置图.
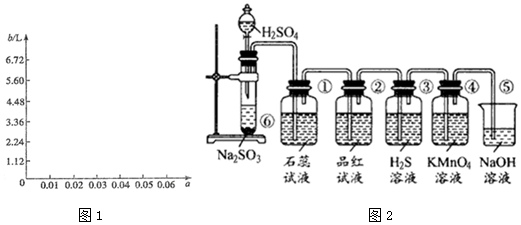
试回答:
Ⅰ.实验中应该选择浓硫酸,是否使用98%的浓H2SO4否(填“是”或“否”),写出⑥中反应化学反应方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑.
Ⅱ.①中的实验现象为变红.
Ⅲ.②中的现象证明SO2具有的化学性质为漂白性.
Ⅳ.③中的实验现象是变浑浊(生成淡黄色沉淀),证明SO2有氧化性.
Ⅴ.④中的实验现象是紫红色褪去,证明SO2有还原性.
Ⅵ.⑤的作用是吸收多余的SO2,防止污染空气.
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 12.60 | 18.90 | 28.98 |
| 二氧化硫的体积/L | 1.12 | 1.68 | 2.24 |
| 硫的质量/g | 1.28 | 1.92 | 2.56 |
(2)根据上表数据分析,该样品A(填选项字母)
A.含有Na2S2O3、Na2SO3和Na2SO4三种成分
B.含有Na2S2O3和Na2SO3两种成分
C.只含有Na2S2O3
(3)求第三份样品中各成分的物质的量.
(4)求所加硫酸的物质的量浓度.
(5)若将63g该样品与一定量的该硫酸溶液微热,回答问题:
①欲计算生成SO2的体积,还需要提供的一个数据是(用a表示该数值,并注明单位)硫酸溶液的体积.当a=0.06时,V(SO2)=5.6;
②(2分)在图1上画出b随a变化的曲线
(6)图2是实验室制取SO2并验证SO2的某些性质的装置图.

试回答:
Ⅰ.实验中应该选择浓硫酸,是否使用98%的浓H2SO4否(填“是”或“否”),写出⑥中反应化学反应方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑.
Ⅱ.①中的实验现象为变红.
Ⅲ.②中的现象证明SO2具有的化学性质为漂白性.
Ⅳ.③中的实验现象是变浑浊(生成淡黄色沉淀),证明SO2有氧化性.
Ⅴ.④中的实验现象是紫红色褪去,证明SO2有还原性.
Ⅵ.⑤的作用是吸收多余的SO2,防止污染空气.
4.下列各组中的离子,能在溶液中大量共存的是( )
| A. | Na+、H+、Cl-、HCO3- | B. | K+、Fe3+、NO3-、SO42- | ||
| C. | Ca2+、H+、C1-、OH- | D. | Na+、Ba2+、CO32-、NO3- |
 ,COS属于极性分子(填“极性”或“非极性”).
,COS属于极性分子(填“极性”或“非极性”).