题目内容
13.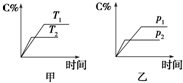 可逆反应A(?)+aB(g)?C(g)+D(g),其中a为正整数.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.试回答下列问题:
可逆反应A(?)+aB(g)?C(g)+D(g),其中a为正整数.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.试回答下列问题:(1)化学方程式中a=1,反应物A的状态是非气态.
(2)该反应的焓变值△H<(填“>”或“<”)0,在不改变其他条件的情况下增加B的物质的量,平衡正(填“正”或“逆”)向移动,平衡常数K不变(填“增大”、“减小”或“不变”).
分析 由左图可知,温度T2到达平衡所用的时间短,故温度T2>T1,温度越高,平衡时C的百分含量(C%)越小,升高温度平衡向逆反应移动,故该反应的正反应为放热反应;
由右图可知,压强P2到达平衡所用的时间短,故压强p2>p1,压强越大,平衡时C的百分含量(C%)越小,增大压强平衡向逆反应移动,故该反应正反应为气体物质的量增大的反应,所以A不是气态.据此结合平衡移动原理解答.
解答 解:由左图可知,温度T2到达平衡所用的时间短,故温度T2>T1,温度越高,平衡时C的百分含量(C%)越小,升高温度平衡向逆反应移动,故该反应的正反应为放热反应;
由右图可知,压强p2到达平衡所用的时间短,故压强p2>p1,压强越大,平衡时C的百分含量(C%)越小,增大压强平衡向逆反应移动,故该反应正反应为气体物质的量增大的反应,所以A不是气态.
(1)压强越大,平衡时C的百分含量(C%)越小,增大压强平衡向逆反应移动,故该反应正反应为气体物质的量增大的反应,A不是气态,逆反应为气体体积减少的反应,故a=1;
故答案为:1;非气态;
(2)由分析可知,该反应的正反应为放热反应,即△H<0;在不改变其他条件的情况下增加B的物质的量,B的浓度增大,平衡向正方向移动,平衡常数只与温度有关,所以平衡常数K不变;
故答案为:<;正;不变.
点评 本题考查了体积分数随温度、压强变化曲线的分析,难度中等,明确“先拐先平数值大”是解本题的关键,注意把握影响化学平衡移动的因素以及影响平衡常数的因素.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
18.已知448℃时反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数是$\frac{1}{7}$,则H2(g)+I2(g)?2HI(g)在该温度下的平衡常数是( )
| A. | $\frac{1}{14}$ | B. | 14 | C. | $\frac{1}{49}$ | D. | 49 |
4.向密闭容器中充入1.0mol CO和2.0mol H2O(g)发生反应:CO+H2O(g)?CO2+H2.当反应达平衡时,CO的转化率为α.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达平衡时CO的转化率小于α的是( )
| A. | 0.5molCO+2.0molH2O(g)+1.0molCO2+1.0mol H2 | |
| B. | 1.0molCO+2.0molH2O(g)+0.5molHe | |
| C. | 1.0molCO+1.0molH2O(g)+1.0molCO2+1.0mol H2 | |
| D. | 0.5molCO+1.5molH2O(g)+0.4molCO2+0.4mol H2 |
5.在恒温恒容的密闭容器中,充入4mol气体A和2mol气体B发生反应:3A(g)+2B(g)?4C(?)+2D(?).反应一段时间后达到平衡,测得生成1.6mol C,反应前后体系压强之比为5:4.则下列说法正确的是( )
| A. | 气体A的平衡转化率大于气体B的平衡转化率 | |
| B. | 物质D的聚集状态一定是气体 | |
| C. | 平衡后升高温度,若平衡向左移动,则正反应的△H>0 | |
| D. | 平衡后若减小该体系的压强,则平衡向左移动,化学平衡常数增大 |
2.下列叙述不正确的是( )
| A. | 对于C(s)+H2O(g)?CO(g)+H2(g)反应,在一定条件下达到平衡,增加或减少C(s)的量平衡不移动 | |
| B. | 对于2SO2(g)+O2(g)?2SO3(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均不能作为达到化学平衡状态的标志 | |
| C. | 对于C(s)+CO2(g)?2CO(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均能作为达到化学平衡状态的标志 | |
| D. | 对于I2(g)+H2(g)?2HI(g)反应,加入催化剂或增大压强均能缩短达到平衡所用时间,但HI的百分含量保持不变 |

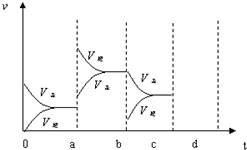 如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升温;b~c过程中改变的条件可能是减小生成物 SO3 的浓度; 若增大压强时,反应速度变化情况画在c~d处.以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).
如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是升温;b~c过程中改变的条件可能是减小生成物 SO3 的浓度; 若增大压强时,反应速度变化情况画在c~d处.以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将(容器不与外界进行热交换,填“升高”或“降低”);达新平衡时,容器内混合气体的平均相对分子质量比原平衡时(填“增大”、“减小”或“相等”).