题目内容
11.某H2SO4试液10.00mL,滴定消耗NaOH标准溶液[c(NaOH)=0.2000mol/L]30.26mL,求该试液中H2SO4的质量浓度.分析 根据滴定和中和氢氧化钠的量根据方程式计算消耗硫酸的物质的量,然后根据c=$\frac{n}{V}$,进行计算求解.
解答 解:消耗NaOH标准溶液[c(NaOH)=0.2000mol/L]30.26mL,所以消耗氢氧化钠的物质的量为:0.2×30.26=6.052mmol,由反应H2SO4+2NaOH=Na2SO4+2H2O可知:n(H2SO4)=$\frac{6.052mmol}{2}$=3.026mmol,则:试液中H2SO4的质量浓度为:$\frac{3.026mmol}{10.00mL}$=0.3026mol/L,答:该试液中H2SO4的质量浓度为:0.3026mol/L.
点评 本题主要考查中和滴定求物质的量浓度,学生只要学会应用公式就可以迅速解题,比较容易.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
19.下列离子方程式与所述事实相符且正确的是( )
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 向NaAlO2溶液中通人过量CO2制Al(OH)3:AlO2-+CO2+H2O═Al(OH)3↓+HCO3- | |
| D. | 向含2molAlCl3的溶液中加入1L 7mol/L的NaOH溶液:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O |
6.下列画有横线的物质在反应中不能完全消耗的是( )
| A. | 将含少量CO2的CO气体通入盛有足量Na2O2的密闭容器中,并不断用电火花引燃 | |
| B. | 将l mol Mg置于10 L空气(标况)中,使之在高温下反应 | |
| C. | 标准状况下,将11.2L H2S与22.4L O2混合点燃 | |
| D. | 在强光持续照射下,向过量的Ca(ClO)2的悬浊液中通入少量CO2 |
16.下列关于Cl2的说法中,不正确的是( )
| A. | Cl2是一种黄绿色、有刺激性气味、有毒的气体 | |
| B. | Cl2能使湿润的红色布条褪色 | |
| C. | Fe在Cl2中燃烧,生成的产物为FeCl2 | |
| D. | 实验室用加热二氧化锰和浓盐酸的方法制取Cl2 |
3.用括号内的试剂可除去各组物质中的少量杂质,使物质得到提纯的是( )
| A. | 乙醇中的水(Na) | B. | 乙酸乙酯中的乙醇(乙酸) | ||
| C. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) | D. | 乙酸中的苯酚(NaOH溶液) |
13.在相同条件下,H2和CO的混合气体VL,完全燃烧时需O2的体积是( )
| A. | 2VL | B. | VL | C. | 0.5VL | D. | 无法计算 |
14.下列物质属于弱电解质的是( )
| A. | CO2 | B. | NH3•H2O | C. | HCl | D. | AgNO3 |
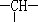 和一个-Cl,它的可能的结构有几种( )
和一个-Cl,它的可能的结构有几种( )