题目内容
3.与标况下11.2L的CO2所含氧原子数相等的水的质量为( )| A. | 44g | B. | 22g | C. | 18g | D. | 9g |
分析 根据n=$\frac{V}{{V}_{m}}$计算出标况下11.2L的CO2的物质的量,然后得出二氧化碳分子中含有氧原子的物质的量,水分子中含有1个氧原子,则水的物质的量与氧原子的物质的量相等,最后根据m=nM计算出水的质量.
解答 解:标况下11.2L的CO2的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,0.5mol二氧化碳分子中含有氧原子的物质的量为:0.5mol×2=1mol,
水分子中含有1个氧原子,则水的物质的量为1mol,质量为:18g/mol×1mol=18g,
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
3.2016年6月25日20时00分,我国新一代运载火箭“长征七号”在海南文昌航天发射场点火升空,首飞成功.“长征七号”运载火箭使用的是液氧煤油推进剂,下列说法不正确的是( )
| A. | 工业上可利用空气冷冻成液体后再分离来获得液氧 | |
| B. | 煤油燃烧后的主要产物是水和二氧化碳,绿色环保 | |
| C. | 煤油属于纯净物.主要成分是烃 | |
| D. | 火箭装载的燃料越多,说明其动力越大 |
4.已知H2CO3:K1=4.3×10-7,K2=5.6×10-11;HCN:K=4.9×10-10,下列说法正确的是( )
| A. | 等浓度NaCN、Na2CO3溶液,pH值:前者>后者 | |
| B. | NaCN溶液中通入少量CO2的离子方程式:2CN-+CO2+H2O=CO32-+2HCN | |
| C. | pH=12的NaOH溶液与pH=5HCN溶液等体积混合后恰好中和,混合后c(Na+)=c(CN-) | |
| D. | 若pH=12的NaOH溶液与pH=5HCN溶液混合后pH=7,则由水电离c(H+)=10-7mol•L-1 |
11.下列物质属于酯类的是①花生油 ②柴油 ③牛油 ④机油⑤汽油 ⑥菜籽油 ⑦煤焦油( )
| A. | ②③④⑦ | B. | ①③⑥ | C. | ⑤⑥⑦ | D. | ②⑤ |
8.如图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是( )
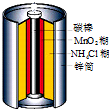

| A. | 电池内部含有电解质 | B. | 锌是负极,碳棒是正极 | ||
| C. | 电子由碳棒经外电路流向锌 | D. | 锌锰干电池属一次电池 |
15.下列物质中,不能使品红溶液褪色的是( )
| A. | 次氯酸 | B. | 臭氧 | C. | 二氧化碳 | D. | 二氧化硫 |
13.同一主族的两种元素的核外电子差值不可能为( )
| A. | 2 | B. | 8 | C. | 18 | D. | 30 |