题目内容
10.下列关于胶体的叙述,不正确的是( )| A. | 胶体中分散质粒子直径大小在1~100 nm之间 | |
| B. | 可以利用丁达尔效应区分胶体和溶液 | |
| C. | 可利用过滤的方法分离胶体和溶液 | |
| D. | 胶体在一定条件下可以稳定存在 |
分析 A.胶体中分散质的微粒直径在1nm~100nm;
B.胶体具有丁达尔效应而溶液不具备;
C.胶体粒子直径大于半透膜孔隙,不可以透过半透膜;
D.胶体是介稳体系.
解答 解:A.胶体中分散质的微粒直径在10-9~10-7m之间,即1nm~100nm,故A正确;
B.胶体和溶液可以用丁达尔现象鉴别,光线通过时胶体出现光亮的通路,溶液无现象,故B正确;
C.胶体和溶液都能透过滤纸,故C错误;
D.胶体是介稳体系,一定条件下能稳定存在,故D正确.
故选C.
点评 本题考查了胶体性质,胶体与其他分散系的本质区别,题目难度不大,熟悉胶体的性质及判断即可解答.

练习册系列答案
相关题目
18.在蒸发皿中加热蒸干再加热(低400℃)下列物质的溶液,可以得到该物质固体的是( )
| A. | AlCl3 | B. | Na2CO3 | C. | Na2SO3 | D. | MgSO4 |
5.下列说法中,正确的是( )
| A. | 1 molCO的质量为28 g | |
| B. | 铁原子的摩尔质量就是铁的相对原子质量 | |
| C. | 标准状况下,任何物质的摩尔体积都约是22.4 L | |
| D. | 1.42 gNa2SO4固体溶于100 mL水中,配得0.10 mol/L的硫酸钠溶液 |
15.以下反应属于氧化还原反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | 2NH4HCO3$\stackrel{△}{→}$2NH3↑+H2O+CO2↑ | ||
| C. | 4HCl+O2$\stackrel{△}{→}$2H2O+2Cl2 | D. | NaHCO3+NaHSO4═Na2SO4+CO2↑+H2O |
2.下列物质中,属于强电解质的是( )
| A. | 酒精 | B. | 二氧化硫 | C. | 一水合氨 | D. | 硫酸钡 |
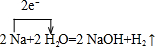 .
.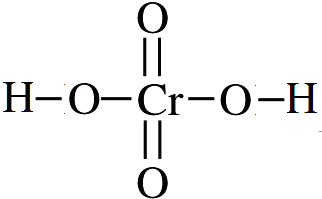 .
.