题目内容
5.研究化学反应常用${\;}_8^{18}$O作为示踪原子,该原子的质子数是( )| A. | 18 | B. | 8 | C. | 10 | D. | 16 |
分析 元素符号的左下角为质子数,据此解题.
解答 解:元素符号的左下角为质子数,${\;}_8^{18}$O的质子数为8,质量数为18.
故选B.
点评 本题考查原子的构成,难度不大,明确核素中的数字的所代表的意义及原子中质子数+中子数=质量数即可解答.

练习册系列答案
相关题目
15.单原子离子R2-含有18个电子,则元素R在周期表的位置是( )
| A. | 第三周期0族 | B. | 第二周期ⅥA族 | C. | 第三周期ⅡA族 | D. | 第三周期ⅥA族 |
16.下列每步转化不能通过一步反应就实现的是( )
| A. | N2→NO→NO2 | B. | Fe→FeCl2→Fe (OH)2 | C. | S→SO3→H2SO4 | D. | Na→Na2O2→NaOH |
20.下列说法正确的是( )
| A. | 第二周期元素的正化合价由+1→+7依次升高 | |
| B. | PH3在空气中可以自燃,根据元素周期律可以推知SiH4很难燃烧 | |
| C. | Cl的非金属性强于S,所以HClO3的酸性一定强于H2SO3 | |
| D. | Li的电子层数小于Al,但是Li的原子半径却却大于Al |
10.下列各组性质比较中,不正确的是( )
| A. | 元素最高化合价:Al>Mg | B. | 金属性:Al>Mg | ||
| C. | 酸性:H2SO4>H3PO4 | D. | 稳定性:HF>HCl |
14.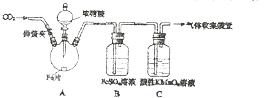 甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
文献记载:Ⅰ.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,气生成的产物有有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO?Fe(NO)SO4(棕色)△H<0
Ⅲ.NO2和NO都能被KMnO4氧化吸收
甲的实验操作和现象记录如下:
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)检验是否生成-3价氮的化合物,应进行的实验操作是取少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口.若试纸变蓝,则A中生成NH4+.
(3)甲取少量B中溶液,加热,实验现象是棕色溶液变浅(或绿),无色气体逸出,且在空气中变为红棕色.甲依据该现象得出的结论是A中有NO生成.请用化学平衡原料解释原因:FeSO4+NO?Fe(NO)SO4(棕色)△H<0正反应放热,加热后,平衡向逆反应方向移动.
(4)乙认为甲得出A中有NO生成的证据不足.为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是浓硝酸换成稀硝酸,此时A中首先发生反应的离子方程式是Fe+4H++NO3-═Fe3++NO↑+2H2O,证明有NO生成的实验现象是A中没有红棕色气体生成,B中溶液变为棕色.
(5)证明A溶液中是否含有Fe2+和Fe3+,选择的药品是(填序号)cd.
a.铁粉 b.溴水 c.铁氰化钾溶液 d.硫氰化钾溶液.
 甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.文献记载:Ⅰ.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,气生成的产物有有+4、+2、-3价等氮的化合物.
Ⅱ.FeSO4+NO?Fe(NO)SO4(棕色)△H<0
Ⅲ.NO2和NO都能被KMnO4氧化吸收
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | / |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余 |
(1)滴入浓硝酸加热前没有明显现象的原因是常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生.
(2)检验是否生成-3价氮的化合物,应进行的实验操作是取少量反应后A中溶液于试管中,向其中加入浓NaOH溶液,加热,用湿润的红色石蕊试纸接近试管口.若试纸变蓝,则A中生成NH4+.
(3)甲取少量B中溶液,加热,实验现象是棕色溶液变浅(或绿),无色气体逸出,且在空气中变为红棕色.甲依据该现象得出的结论是A中有NO生成.请用化学平衡原料解释原因:FeSO4+NO?Fe(NO)SO4(棕色)△H<0正反应放热,加热后,平衡向逆反应方向移动.
(4)乙认为甲得出A中有NO生成的证据不足.为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是浓硝酸换成稀硝酸,此时A中首先发生反应的离子方程式是Fe+4H++NO3-═Fe3++NO↑+2H2O,证明有NO生成的实验现象是A中没有红棕色气体生成,B中溶液变为棕色.
(5)证明A溶液中是否含有Fe2+和Fe3+,选择的药品是(填序号)cd.
a.铁粉 b.溴水 c.铁氰化钾溶液 d.硫氰化钾溶液.
15.下列字母表示短周期中几种元素的位置,请回答下列问题.
(1)D2-的离子结构示意图为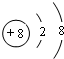 ,E与I形成的化合物的电子式为
,E与I形成的化合物的电子式为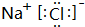 .
.
(2)E,G,H三元素的最高价氧化物对应水化物的溶液间相互反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O,OH-+H+=H2O.
(3)F和I形成的化合物中存在的化学键类型是离子键,在A~I九种元素中,完全由非金属元素形成的一个离子化合物的化学式是NH4NO3.
(4)4.8g单质F能与标准状况下2.24L的B的最高价氧化物恰好反应.
| A | |||||||
| B | C | D | |||||
| E | F | G | H | I | |||
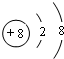 ,E与I形成的化合物的电子式为
,E与I形成的化合物的电子式为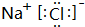 .
.(2)E,G,H三元素的最高价氧化物对应水化物的溶液间相互反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O,OH-+H+=H2O.
(3)F和I形成的化合物中存在的化学键类型是离子键,在A~I九种元素中,完全由非金属元素形成的一个离子化合物的化学式是NH4NO3.
(4)4.8g单质F能与标准状况下2.24L的B的最高价氧化物恰好反应.