题目内容
20.下列情况能通过置换反应得到铁的是( )| A. | Cu与FeCl 3溶液混合 | B. | CO通过灼热的Fe 2O 3 | ||
| C. | H 2通入FeSO 4溶液 | D. | Al和Fe 3O 4混合加热至高温 |
分析 A.Cu与氯化铁发生氧化还原反应生成氯化铜、氯化亚铁;
B.反应生成Fe和二氧化碳;
C.二者不发生反应;
D.发生铝热反应生成Fe和氧化铝.
解答 解:A.Cu与氯化铁发生氧化还原反应生成氯化铜、氯化亚铁,生成物中无单质Fe,故A不选;
B.反应生成Fe和二氧化碳,反应物中无单质,不是置换反应,故B不选;
C.二者不发生反应,不能得到Fe,故C不选;
D.发生铝热反应生成Fe和氧化铝,为单质与化合物反应生成新单质、化合物的反应,属于置换反应,故D选;
故选D.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
10.在2L的密闭容器中发生如下反应:3A+B=C+D,若开始时加入的A和B均是4mol,在前10s内A的平均反应速率为0.12mol/(L•S),则10S时容器内C的物质的量为( )
| A. | 3.2mol | B. | 2.4mol | C. | 0.8mol | D. | 0.4mol |
11.下列有关化学反应方向及其判据的说法中错误的是( )
| A. | 1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | |
| B. | 凡是放热反应都是自发的,因为吸热反应都是非自发的 | |
| C. | CaCO3(s)?CaO(s)+CO2(g)△H>0 能否自发进行与温度有关 | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
8.下列有关物质性质的说法错误的是( )
| A. | 热稳定性:HCl>HI | B. | 结合质子能力:S2->Cl- | ||
| C. | 原子半径:Ge>As | D. | 酸性:HNO2>HNO3 |
15. 在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
 在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )| A. | 含有碳碳双键、羟基、羰基、羧基 | B. | 含有苯基、羟基、羰基、羧基 | ||
| C. | 含有羟基、羰基、羧基、酯基 | D. | 含有碳碳双键、苯基、羟基、羰基 |
5.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成过程.已知键能数据如表:
反应N2(g)+3H2(g)?2NH3(g);△H=-93kJ•mol-1.试根据表中所列键能数据计算b数值( )
| 化学键 | N≡N | N-H | H-H |
| 键能(kJ/mol) | 942 | 391 | b |
| A. | 551 | B. | 437 | C. | 558 | D. | 160 |
9.苯环实际上不具有碳碳单键和双键的交替结构,可以作为证据的事实有( )
①苯的间位二取代物只有一种
②苯的邻位二取代物只有一种
③苯分子中碳碳键的键长均相等
④苯不能使酸性KMnO4溶液褪色
⑤苯在加热和催化剂存在条件下,与氢气发生加成反应
⑥苯在FeBr3存在的条件下,与液溴发生取代反应,但不能因化学变化而使溴水褪色.
①苯的间位二取代物只有一种
②苯的邻位二取代物只有一种
③苯分子中碳碳键的键长均相等
④苯不能使酸性KMnO4溶液褪色
⑤苯在加热和催化剂存在条件下,与氢气发生加成反应
⑥苯在FeBr3存在的条件下,与液溴发生取代反应,但不能因化学变化而使溴水褪色.
| A. | ①②③④ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | 全部 |
1.研究小组同学对金属镁与NH4Cl溶液的反应产生了浓厚的兴趣.可供选择的实验试剂为:镁粉,1mol/L NH4Cl溶液,1mol/L盐酸溶液,1.0mol/LCH3COONH4溶液,1.0mol/LKNO3溶液,1.0mol/LNaCl溶液
(1)研究小组做了如下几组实验,请完成下面表格(表中不要留空格):
从实验结果得知,常温下镁几乎不和水反应,却很容易与NH4Cl,NH4NO3溶液反应产生气体,实验②的目的是验证铵根离子能和镁反应,但同学们认为这个方案还应该补充:NaNO3溶液与镁作用.
(2)研究小组提出如下猜测:
假设一:NH4+是这个反应的催化剂,能促进水和镁反应:
假设二:Cl-是镁和水反应的催化剂;
假设三:NH4+水解溶液呈酸性…
请写出NH4Cl水解反应离子反应方程式:NH4++H2O?NH3•H2O+H+.
(3)研究小组发现除了生产氢气外,还生成了能使湿润的红色石蕊试纸测变蓝的气体.请简写出用试纸测试气体的过程取湿润的红色石蕊试纸粘在玻璃棒上,靠近出气口,试纸变蓝,说明生成氨气(4)为验证假设二,请你设计一个实验方案,写出实验步骤和结论.
(1)研究小组做了如下几组实验,请完成下面表格(表中不要留空格):
| 编号 | 镁粉/g | H2O/mL | NH4Cl溶液/mL | NH4NO3溶液/mL |
| ① | 5 | 0 | 20 | 0 |
| ② | 5 | 0 | 0 | 20 |
| ③ | 5 | 20 | 0 | 0 |
(2)研究小组提出如下猜测:
假设一:NH4+是这个反应的催化剂,能促进水和镁反应:
假设二:Cl-是镁和水反应的催化剂;
假设三:NH4+水解溶液呈酸性…
请写出NH4Cl水解反应离子反应方程式:NH4++H2O?NH3•H2O+H+.
(3)研究小组发现除了生产氢气外,还生成了能使湿润的红色石蕊试纸测变蓝的气体.请简写出用试纸测试气体的过程取湿润的红色石蕊试纸粘在玻璃棒上,靠近出气口,试纸变蓝,说明生成氨气(4)为验证假设二,请你设计一个实验方案,写出实验步骤和结论.
| 实验步骤(不要求写出具体操作过程): 增加一组镁与NaCl溶液的作用的实验 实验结论常温下镁几乎不和NaCl溶液反应 |
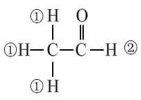 已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.
已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.