题目内容
1.下列关于12C和13C说法正确的是( )| A. | 两者互为同位素 | B. | 两者属于不同的元素 | ||
| C. | 两者属于同一种核素 | D. | 两者互为同素异形体 |
分析 A.具有相同质子数,不同中子数的不同原子互为同位素;
B.元素的种类由质子数决定;
C.核素是指具有一定数目质子和一定数目中子的一种原子;
D.同素异形体是由同一种元素组成的不同单质.
解答 解:A.12C和13C是质子数相同,中子数不同的原子,互为同位素,故A正确;
B.12C和13C质子数相同,中子数不同,是碳元素不同核素,都属于碳元素,故B错误;
C.12C和13C中子数不同,是碳元素的不同核素,故C错误;
D.12C和13C是原子,不是单质,故D错误;
故选A.
点评 本题考查同位素、同素异形体、核素、元素的概念,比较基础,注意把握概念的内涵与外延.

练习册系列答案
相关题目
11.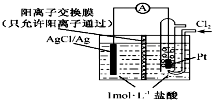 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )| A. | 正极反应为AgCl+e-=Ag+Cl- | |
| B. | 电池工作时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 若用KCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子 |
12.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | 人们可以把放热反应释放的能量转化为其它可利用的能量,而吸热反应没有利用价值 | |
| B. | 太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用 | |
| C. | 地球上最基本的能源是化学能 | |
| D. | 利用二氧化碳制造全降解塑料能有效减少“白色污染” |
9.下列各组微粒中,互为等电子体的一组是( )
| A. | CO、C2H2、N2 | |
| B. | SO2、NO${\;}_{2}^{+}$、N${\;}_{3}^{-}$、CNO- | |
| C. | CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$、BeCl2 | |
| D. | SiF4、SiO${\;}_{4}^{4-}$、SO${\;}_{4}^{2-}$、PO${\;}_{4}^{3-}$ |
16.mmol C2H4跟 nmol H2在密闭容器中反应,生成pmol C2H6.将反应后的混合气体完全燃烧,生成CO2和H2O,所需氧气的物质的量是( )
| A. | 3.5 pmol | B. | (3m+$\frac{n}{2}$-3p)mol | C. | (3m+$\frac{n}{2}$)mol | D. | (3m+n)mol |
13.对于300mL 1mol•L-1盐酸与铁片的反应,采取下列措施:
①升高温度
②改用100mL 3mol•L-1盐酸
③再加300mL 1mol•L-1盐酸
④用等量铁粉代替铁片
⑤改用100mL 98%的硫酸
其中能使反应速率加快的是( )
①升高温度
②改用100mL 3mol•L-1盐酸
③再加300mL 1mol•L-1盐酸
④用等量铁粉代替铁片
⑤改用100mL 98%的硫酸
其中能使反应速率加快的是( )
| A. | ①②④ | B. | ①③④ | C. | ①②③④ | D. | ①②③⑤ |
10.A和B是短周期元素,A2-和B+的核外电子总数之差为8,A的原子序数大于B,下列说法中正确的是( )
| A. | A和B的原子序数之差为8 | B. | A和B原子最外层电子数之和为8 | ||
| C. | A和B原子最外层电子数之和为3 | D. | A、B原子核外电子数总和可能为11 |
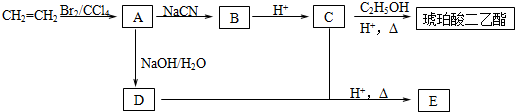
 +2nH2O.
+2nH2O.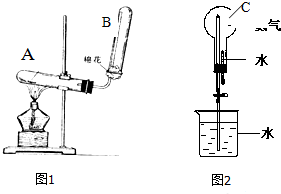 图(1、2)是有关氨的制取和性质的实验装置.
图(1、2)是有关氨的制取和性质的实验装置.