题目内容
常温下,取0.2mol?L-1 HCl溶液与0.2mol?L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)混合溶液中由水电离出的c(H+) 0.2mol?L-1 HCl溶液中由水电离出的c(H+)(填“>、<或=”).
(2)求出混合物中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)= mol?L-1,c(H+)-c(MOH)= mol?L-1.
(3)若常温下取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,测得混合溶液的pH<7,说明MOH的电离程度 (填“>、<或=”)MCl的水解程度.溶液中各离子浓度由大到小的顺序为 .
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,则混合溶液的pH 7(填“>、<或=”).
(1)混合溶液中由水电离出的c(H+)
(2)求出混合物中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=
(3)若常温下取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,测得混合溶液的pH<7,说明MOH的电离程度
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,则混合溶液的pH
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)室温下取0.2mol?L-1HCl溶液与0.2mol?L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,说明得到的盐是强酸弱碱盐,其溶液呈酸性,含有弱根离子的盐促进水电离;
(2)根据物料守恒和电荷守恒计算离子浓度大小;
(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,根据电荷守恒判断离子浓度大小;
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,氨水为弱碱,混合后氨水过量,溶液显示碱性.
(2)根据物料守恒和电荷守恒计算离子浓度大小;
(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,根据电荷守恒判断离子浓度大小;
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,氨水为弱碱,混合后氨水过量,溶液显示碱性.
解答:
解:(1)等体积等浓度的盐酸和MOH恰好反应生成盐,得到的盐溶液呈酸性,说明该盐是强酸弱碱盐,含有弱根离子的盐促进水电离,酸抑制水电离,所以混合溶液中水电离出的c(H+)>0.2 mol?L-1 HCl溶液中水电离出的c(H+),
故答案为:>;
(2)根据电荷守恒得c(Cl-)-c(M+)=c(H+)-c(OH-)=10-6 mol/L-10-8 mol/L=9.9×10-7mol?L-1,根据质子守恒得 c(H+)-c(MOH)=c(OH-)=1.0×10-8mol?L-1,
故答案为:9.9×10-7;1.0×10-8;
(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒知c(Cl-)>c(M+),盐中阴阳离子浓度大于氢离子和氢氧根离子浓度,所以溶液中各离子浓度由大到小的顺序为c(Cl-)>c(M+)>c(H+)>c(OH-),
故答案为:<;c(Cl-)>c(M+)>c(H+)>c(OH-);
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,氨水的浓度大于0.001mol/L,而盐酸的浓度为0.001mol/L,等体积混合后氨水过量,溶液显示碱性,溶液的pH>7,
故答案为:>.
故答案为:>;
(2)根据电荷守恒得c(Cl-)-c(M+)=c(H+)-c(OH-)=10-6 mol/L-10-8 mol/L=9.9×10-7mol?L-1,根据质子守恒得 c(H+)-c(MOH)=c(OH-)=1.0×10-8mol?L-1,
故答案为:9.9×10-7;1.0×10-8;
(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒知c(Cl-)>c(M+),盐中阴阳离子浓度大于氢离子和氢氧根离子浓度,所以溶液中各离子浓度由大到小的顺序为c(Cl-)>c(M+)>c(H+)>c(OH-),
故答案为:<;c(Cl-)>c(M+)>c(H+)>c(OH-);
(4)若常温下pH=3的盐酸与pH=11的氨水溶液等体积混合,氨水的浓度大于0.001mol/L,而盐酸的浓度为0.001mol/L,等体积混合后氨水过量,溶液显示碱性,溶液的pH>7,
故答案为:>.
点评:本题考查酸碱混合的定性判断和计算,为高频考点,侧重于学生的分析能力和计算能力的考查,根据电荷守恒和质子守恒分析弱电解质的电离及盐类水解,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中存在顺反异构体的是( )
| A、1,2-二氯乙烯 |
| B、2-甲基丙烯 |
| C、2-甲基-2-丁烯 |
| D、1-丁烯 |
下列各组中的反应,属于同一反应类型的是( )
| A、由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 |
| B、由甘油和浓硝酸制硝化甘油炸药;由甲苯和浓硝酸制TNT炸药 |
| C、由氯代环己烷消去制环己烯;由丙烯加溴制1,2-二溴丙烷 |
| D、由乙醇和浓硫酸共热制乙醚;由乙醇和浓硫酸共热制乙烯 |
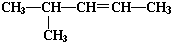
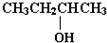
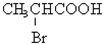
 如图有机物A的分子,所含有的官能团的名称是
如图有机物A的分子,所含有的官能团的名称是