题目内容
下列离子方程式正确的是( )
| A、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、铝粉没入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、铁与盐酸反应:Fe+2H+═Fe3++H2↑ |
| D、Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸;
B、选项中原子不守恒,电子不守恒;
C、铁和盐酸反应生成氯化亚铁和氢气;
D、氢氧化钡和硫酸反应生成硫酸钡沉淀和水.
B、选项中原子不守恒,电子不守恒;
C、铁和盐酸反应生成氯化亚铁和氢气;
D、氢氧化钡和硫酸反应生成硫酸钡沉淀和水.
解答:
解:A、氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸,氯气溶于水:Cl2+H2O═H++Cl-+HClO,故A错误;
B、选项中原子不守恒,电子不守恒,铝粉投入到NaOH溶液中:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、铁和盐酸反应生成氯化亚铁和氢气,铁与盐酸反应的离子方程式:Fe+2H+═Fe2++H2↑,故C错误;
D、氢氧化钡和硫酸反应生成硫酸钡沉淀和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D正确;
故选D.
B、选项中原子不守恒,电子不守恒,铝粉投入到NaOH溶液中:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、铁和盐酸反应生成氯化亚铁和氢气,铁与盐酸反应的离子方程式:Fe+2H+═Fe2++H2↑,故C错误;
D、氢氧化钡和硫酸反应生成硫酸钡沉淀和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D正确;
故选D.
点评:本题考查了离子方程式书写方法和注意问题,主要是原子守恒、电子守恒分析应用,注意次氯酸是弱酸,题目较简单.

练习册系列答案
相关题目
形形色色的硅酸盐存在于地球的每一个角落,在人类的生活和生产中扮演着重要的角色,下列说法不正确的是( )
| A、古代的陶瓷、砖瓦,现代的玻璃、水泥等,都是硅酸盐产品 |
| B、硅晶体的导电性介于导体和绝缘体之间,是一种重要的半导体材料 |
| C、硅酸、二氧化硅、硅酸钠及硅酸盐产品均属于电解质 |
| D、青花瓷胎体的原料为高岭土[Al2Si2O5(OH)4],若以氧化物形式科表示为:Al2O3?2SiO2?2H2O |
NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、含0.1mol BaCl2的溶液中Cl-数为0.2NA |
| B、22g CO2所含有的分子数为0.5NA 已知M(CO2)=44g/mol |
| C、11.2L CO2所含有的分子数为0.5NA |
| D、常温下NA个N2分子电子数为14NA |
下列表达方式不正确的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式  | ||
C、S2-离子的结构示意图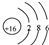 | ||
D、镁-24原子
|
在标准状况下,相同质量的下列气体体积最大的是( )
| A、CH4 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
下列各图中,表示正反应是放热反应的图是.( )
A、 |
B、 |
C、 |
D、 |
元素周期律的发现对新元素的发现、化学理论和实验等研究工作起到了指导作用.周期律揭示的规律包括以下内容中的( )
①元素的性质随原子序数的递增呈周期性变化
②元素的性质是元素原子序数的周期性函数
③事物的量变可以引起质变
④元素性质的递变是原子核外电子排布的必然结果.
①元素的性质随原子序数的递增呈周期性变化
②元素的性质是元素原子序数的周期性函数
③事物的量变可以引起质变
④元素性质的递变是原子核外电子排布的必然结果.
| A、①② | B、①③ |
| C、①④ | D、①②③④ |
下列化工生产过程所发生的反应不属于氧化还原反应的是( )
| A、用氯气和消石灰制漂白粉 |
| B、用纯碱、石灰石和石英制普通玻璃 |
| C、用石油炼制过程脱硫得到的硫磺制造硫酸 |
| D、用金属钠从四氯化钛(TiCl4)中提炼金属钛 |
下列说法正确的是( )
| A、化学反应不一定都有反应热 |
| B、使用催化剂可以改变反应的平衡常数 |
| C、升高温度使反应加快,是因为降低了反应的活化能 |
| D、对于同一个化学反应无论是一步完成还是分几步完成,其反应的焓变相同 |