题目内容
4.按要求回答下列问题(1)已知反应:mA(g)+nB(g)?pC(g)+qD(g),v(A):v(B)=m:n;
(2)任何情况下判断水溶液呈中性的依据是:c(OH-)=c(H+);
(3)NH4Cl溶液中离子浓度由大到小的顺序是:c(Cl-)>c(NH4+)>c(H+)>c(OH-).
分析 (1)化学反应速率与化学计量数成正比;
(2)水溶液中,水电离的氢离子与氢氧根离子的浓度相等,则溶液显示中性;
(3)氯化铵溶液中,铵根离子部分水解,溶液显示酸性,c(H+)>c(OH-),再结合电荷守恒判断各离子浓度大小.
解答 解:(1)反应mA(g)+nB(g)?pC(g)+qD(g)中,A、B的反应速率与其计量数成正比,则v(A):v(B)=m:n,
故答案为:m:n;
(2)任何纯水溶液中,水电离的氢离子与氢氧根离子的物质的量浓度相等,即:c(OH-)=c(H+),所以水溶液一定为中性,
故答案为:c(OH-)=c(H+);
(3)氯化铵溶液中铵根离子部分水解:NH4++H2O=NH3•H2O+H+,则:c(H+)>c(OH-)、c(Cl-)>c(NH4+),溶液中离子浓度由大到小顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-).
点评 本题考查了离子浓度大小比较、化学反应速率的计算、水的电离及其应用等知识,题目难度中等,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用方法,明确化学反应速率与化学计量数的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.化学与生活、生产密切相关,下列过程没有发生化学反应的是( )
| A. | 对肾功能衰竭病人进行“血液透析” | |
| B. | 用热的纯碱溶液清除餐具上沾有的油污 | |
| C. | 常温下用铝罐贮藏贮运浓硫酸 | |
| D. | 对石油进行分馏,裂化获得汽油 |
15.某元素R的最高价氧化物的化学式为RO2,且R的气态氢化物中氢的质量分数为25%,此元素是( )
| A. | C | B. | N | C. | Si | D. | P |
12.X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法不正确的是( )
| A. | Y元素最高价氧化物对应水化物的化学式为HYO4 | |
| B. | 原子半径由小到大的顺序为W<X<Z | |
| C. | X与W可形成W2X、W2X2两种物质 | |
| D. | Y2与W2在冷暗处爆炸 |
19.用惰性电极电解下列溶液的说法正确是( )
| A. | 电解氯化钾溶液的过程中,溶液的pH变小 | |
| B. | 电解硝酸银溶液的过程中,阴极质量不变,阳极质量增大 | |
| C. | 电解硫酸钠溶液的过程中,两极产生气体的物质的量不相同 | |
| D. | 电解氢氧化钠溶液的过程中,氢氧化钠的物质的量浓度减小 |
9.下列有关表示正确的是( )
| A. | 氯化氢分子的电子式: | B. | 氯离子的结构示意图: | ||
| C. | 乙烯分子的结构式:CH2=CH2 | D. | 苯分子的比例模型: |
16.下列物质不能使酸性KMnO4溶液褪色的是( )
| A. |  | B. | C2H2 | C. |  | D. | 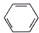 |
13.下列各组有机物只用一种试剂无法鉴别的是( )
| A. | 甲酸、乙醛、乙酸 | B. | 苯、苯酚、己烯 | ||
| C. | 乙醇、四氯化碳、乙酸乙酯 | D. | 苯、甲苯、环己烷 |
14.下列有机物分子中,所有原子不可能处于同一平面的是( )
| A. |  | B. | CH2=CH-CH=CH2 | C. |  | D. |  |