题目内容
16.表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)元素⑤的氢氧化物与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
(3)用电子式表示元素④与⑦的化合物的形成过程:
 .
.
分析 由元素在周期表的位置可知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)稀有气体化学性质稳定,F的非金属性最强;
(2)氢氧化铝与盐酸反应生成氯化铝与水;
(3)元素④与⑦的化合物为NaCl,为离子化合物.
解答 解:由元素在周期表的位置可知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)在这些元素中,化学性质最不活泼的是Ar,非金属性最强的是F,故答案为:Ar;F;
(2)氢氧化铝与盐酸反应生成氯化铝与水,离子反应方程式为Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O;
(3)元素④与⑦的化合物为NaCl,为离子化合物,用电子式表示形成过程为 ,
,
故答案为: .
.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素的性质、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
6.【物质结构与性质】.
X、Y、Z、W、J是元素周期表前四周期中的五种常见元素.其相关信息如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是146C;
(2)元素Y位于元素周期表第三周期第VIA族;
(3)元素Z的原子最外层共有7种不同运动状态的电子;基态Z原子中,电子占有的最高能层符号为3p;
(4)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1,W的基态原子核外价电子排布图是 ;
;
(5)元素Y与元素Z相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bce;
a.常温下,Y的单质与Z的单质状态不同
b.Z的电负性大于Y
c.Z的氢化物比Y的氢化物稳定
d.在反应中,Y原子得电子数比Z原子得电子数多
e.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)J的元素名称氮,在周期表中位于p区.写出J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的离子方程式NH3+H+=NH4+.
X、Y、Z、W、J是元素周期表前四周期中的五种常见元素.其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
(2)元素Y位于元素周期表第三周期第VIA族;
(3)元素Z的原子最外层共有7种不同运动状态的电子;基态Z原子中,电子占有的最高能层符号为3p;
(4)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1,W的基态原子核外价电子排布图是
 ;
;(5)元素Y与元素Z相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bce;
a.常温下,Y的单质与Z的单质状态不同
b.Z的电负性大于Y
c.Z的氢化物比Y的氢化物稳定
d.在反应中,Y原子得电子数比Z原子得电子数多
e.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)J的元素名称氮,在周期表中位于p区.写出J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的离子方程式NH3+H+=NH4+.
7.反应A+3B=2C+D在以下表示的反应速率中,速率最大的是( )
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) | ||
| C. | v(C)=0.5mol/(L•min) | D. | v (D)=0.45mol/(L•min) |
4.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 2.3gNa在足量O2中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,5.6 L NH3中含有的氢原子数目为0.75NA | |
| C. | 1L0.1mol/LH3PO4溶液中含有的离子数目为0.4NA | |
| D. | 1个C02分子的质量为$\frac{44}{N_A}g$ |
11.燃烧质量相同的下列烃,消耗氧气的物质的量最少的是( )
| A. | CH4 | B. | C2H4 | C. | C4H6 | D. | C6H6 |
5.利用下列实验装置不能完成相应实验的是( )
| A. | 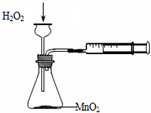 定量测定化学反应速率 | B. | 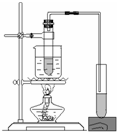 实验室制乙酸丁酯 | ||
| C. | 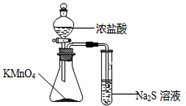 比较KMnO4、Cl2、S的氧化性 | D. | 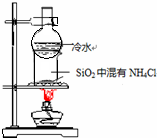 分离SiO2和NH4Cl |
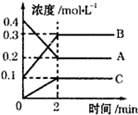 如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题:
如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题: 2B+C.
2B+C.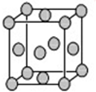 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题.
某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题. .填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).
.填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).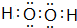 ,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.
,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.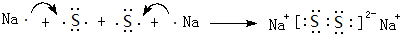 .
.