题目内容
4.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )| A. | 2.3gNa在足量O2中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,5.6 L NH3中含有的氢原子数目为0.75NA | |
| C. | 1L0.1mol/LH3PO4溶液中含有的离子数目为0.4NA | |
| D. | 1个C02分子的质量为$\frac{44}{N_A}g$ |
分析 A、求出钠的物质的量,然后根据钠反应后变为+1价来分析;
B、求出氨气的物质的量,然后根据1mol氨气中含3molH原子来分析;
C、磷酸为中强酸,不能完全电离;
D、1mol二氧化碳的质量为44g,含NA个二氧化碳分子.
解答 解:A、2.3g钠的物质的量为0.1mol,而钠反应后变为+1价,故0.1mol钠反应后转移0.1NA个电子,故A正确;
B、标况下5.6L氨气的物质的量为0.25mol,而1mol氨气中含3molH原子,故0.25mol氨气中含0.75NA个H原子,故B正确;
C、磷酸为中强酸,不能完全电离,故溶液中的离子个数小于0.4NA个,故C错误;
D、1mol二氧化碳的质量为44g,含NA个二氧化碳分子,即NA个二氧化碳分子的质量之和为44g,故每个二氧化碳分子的质量为$\frac{44}{{N}_{A}}$g,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
12.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)③的元素符号是Be,①的元素名称是氧.
(2)在这8种元素的最高价氧化物的水化物中,酸性最强的化合物的名称是高氯酸.②与⑤形成的化合物的电子式是: ,属离子化合物(填“离子”或“共价”).
,属离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用分子式表示)NH3>PH3.
(4)写出⑥最高价氧化物对应水化物跟⑧的最高价氧化物反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(5)请设计实验比较单质②⑧的金属性,写出简单的实验步骤和现象:取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,镁与盐酸反应比铝剧烈.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.89 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +2 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是Be,①的元素名称是氧.
(2)在这8种元素的最高价氧化物的水化物中,酸性最强的化合物的名称是高氯酸.②与⑤形成的化合物的电子式是:
 ,属离子化合物(填“离子”或“共价”).
,属离子化合物(填“离子”或“共价”).(3)比较④和⑦的氢化物的稳定性(用分子式表示)NH3>PH3.
(4)写出⑥最高价氧化物对应水化物跟⑧的最高价氧化物反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(5)请设计实验比较单质②⑧的金属性,写出简单的实验步骤和现象:取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,镁与盐酸反应比铝剧烈.
19.下列实验过程中,未涉及氧化还原反应的是( )
| A. | 粗盐提纯 | B. | 海带提碘 | C. | 氯气溶于水 | D. | 电解水 |
16.表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar,非金属性最强的是F(填具体元素符号,下同).
(2)元素⑤的氢氧化物与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
(3)用电子式表示元素④与⑦的化合物的形成过程: .
.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)元素⑤的氢氧化物与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
(3)用电子式表示元素④与⑦的化合物的形成过程:
 .
.
13.生活中处处有化学.下列相关表述正确的是( )
| A. | 天然橡胶的主要成分是异戊二烯 | |
| B. | 通过物理变化将煤气化和液化,能高效清洁地用煤 | |
| C. | 苯酚能用于环境消毒 | |
| D. | 乙醇是不可再生的能源 |
14.下列有关试剂存放或实验操作正确的是( )

| A. | 液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 | |
| B. | 用湿润的红色石蕊试纸检验酸性气体 | |
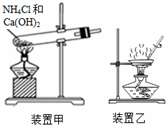
| C. | 用装置甲制备氨气 | |
| D. | 用装置乙加热分解Al(OH)3固体 |