题目内容
7.用下列实验装置进行相应实验,能达到实验目的是( )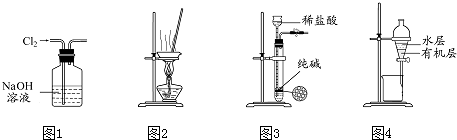
| A. | 用图1 所示装置除去Cl2中含有的少量HCl | |
| B. | 用图2 所示装置蒸干NH4HCO3饱和溶液制备NH4HCO3晶体 | |
| C. | 用图3 所示装置制取少量纯净的CO2气体 | |
| D. | 用图4 所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
分析 A.二者均与NaOH反应;
B.蒸干NH4HCO3饱和溶液,NH4HCO3分解;
C.纯碱为粉末固体,与盐酸接触后关闭止水夹不能使固体、液体分离;
D.CCl4萃取碘水后,水在上层,碘溶解在四氯化碳中、且在下层.
解答 解:A.二者均与NaOH反应,不能除杂,应选饱和食盐水、洗气,故A错误;
B.蒸干NH4HCO3饱和溶液,NH4HCO3分解,应选冷却结晶法,故B错误;
C.纯碱为粉末固体,与盐酸接触后关闭止水夹不能使固体、液体分离,且盐酸易挥发,图中装置不能制取少量纯净的CO2气体,故C错误;
D.CCl4萃取碘水后,水在上层,碘溶解在四氯化碳中、且在下层,利用分液漏斗可分液,图4 所示装置可分离CCl4萃取碘水后已分层的有机层和水层,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、混合物分离提纯、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,22.4L庚烷完全燃烧所生成的气态产物的分子数为7 NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9 NA | |
| C. | 1mol乙烯分子中含有极性键数为4 NA | |
| D. | 1 mol醛基(-CHO)中含有的共用电子数为6 NA |
18.现有4.9gMgO、Mg(OH)2的固体混合物,与l00g9.8%的稀H2SO4恰好完全反应,形成不饱和溶液.则原固体混合物中镁元素的质量为( )
| A. | 1.2g | B. | 1.6g | C. | 2.4g | D. | 4.8g |
15.使用氢氧燃料电池的公共汽车已在北京街头出现.某种以30%KOH溶液为电解质的氢氧燃料电池在使用时的电极反应如下:
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能 | |
| D. | 氢氧燃料电池不属于环境友好电池 |
2.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 点燃 |
| B | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铜粉 |
| C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
| D | 鉴别硬水和软水 | 加入肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
12.某些保健品中含有的锗元素(Ge)位于周期表的第四周期IVA族.有关锗的叙述不正确的是( )
| A. | 锗的原子序数为24 | B. | 锗的金属活动性应比硅强 | ||
| C. | Ge可以生成化学式为Na2GeO3的盐 | D. | 单质锗是半导体材料 |
19.合成氨反应N2+3H2$?_{△}^{Fe}$2NH3,其化学反应速率可以用v(H2)、v(N2)、v(NH3)来表示,单位[mol/(L•s)],那么正确的关系式是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=3v(N2) | C. | v(NH3)=1.5v(H2) | D. | v(N2)=2v(H2) |
16.某烃的相对分子质量小于70,1mol该烃最多可与2mol H2发生加成反应,加成产物最多能与10mol Cl2发生取代反应,则该烃的分子式为( )
| A. | C3H6 | B. | C3H4 | C. | C4H6 | D. | C5 H8 |