题目内容
12.某些保健品中含有的锗元素(Ge)位于周期表的第四周期IVA族.有关锗的叙述不正确的是( )| A. | 锗的原子序数为24 | B. | 锗的金属活动性应比硅强 | ||
| C. | Ge可以生成化学式为Na2GeO3的盐 | D. | 单质锗是半导体材料 |
分析 锗元素(Ge)位于周期表的第四周期IVA族,最高正价为+4价,位于Si 的下方,金属与非金属的交界处,原子序数为14+18=32,同主族从上到下金属性增强,以此来解答.
解答 解:A.Ge在第四周期IVA族,位于Si 的下方,原子序数为14+18=32,故A错误;
B.同主族从上到下金属性增强,则锗的金属活动性应比硅强,故B正确;
C.最高正价为+4价,Ge可以生成化学式为Na2GeO3的盐,故C正确;
D.位于金属与非金属的交界处,单质锗是半导体材料,故D正确;
故选A.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意周期表的指导作用,题目难度不大.

练习册系列答案
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
2.下列说法正确的是( )
| A. | 金属元素与非金属元素形成的化合物一定是离子化合物 | |
| B. | 原子最外层电子数为2的元素一定处于周期表 IIA族 | |
| C. | 离子化合物中不可能存在共价键 | |
| D. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5 |
3.由甲酸甲酯、葡萄糖、乙醛、丙酸四种物质组成的混合物,已知其中氧元素的质量分数为37%,则氢元素的质量分数为( )
| A. | 9% | B. | 12% | C. | 16% | D. | 21% |
20.某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为197.0,原子核外的电子数为97.下列叙述错误的是( )
| A. | 它是副族元素 | |
| B. | 它是第七周期元素 | |
| C. | 它的原子核内有97个质子 | |
| D. | 它的一种同位素的核内有108个中子 |
7.用下列实验装置进行相应实验,能达到实验目的是( )
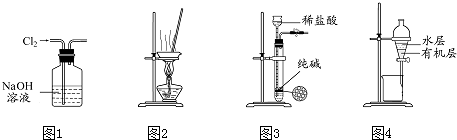

| A. | 用图1 所示装置除去Cl2中含有的少量HCl | |
| B. | 用图2 所示装置蒸干NH4HCO3饱和溶液制备NH4HCO3晶体 | |
| C. | 用图3 所示装置制取少量纯净的CO2气体 | |
| D. | 用图4 所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
17.用短线“-”表示共用电子对,用“‥”表示未成键孤对电子的式子叫路易斯结构式.以下路易斯结构式表示的分子属极性分子的是( )
①
②
③
④
①

②

③

④

| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ③④ |
4.有6克含杂质的Na2SO3与足量盐酸反应,得气体1.12升(STP),且该气体的平均相对分组质量为60,则杂质可能是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | Na2CO3和NaHCO3 | D. | Na2SO4 |
1.瓦斯中甲烷和氧气的质量比为1:4时极易发生爆炸.此时甲烷与氧气的下列物理量之比也为1:4的是( )
| A. | 物质的量之比 | B. | 体积比 | C. | 碳、氧原子个数比 | D. | 氢、氧原子个数比 |
15.下列叙述正确的是( )
| A. | 2.8 g乙烯与丙烯的混合物中含碳原子的数目为0.2NA | |
| B. | 等物质的量的氢氧根离子(OH-)与羟基(-OH)所含电子数相等 | |
| C. | 常温常压下28 g CO与22.4 L O2所含分子数相等 | |
| D. | 16 g CH4与18 g NH4+所含质子数相等 |