题目内容
11.东汉成书的《神农本草经》有“石胆能化铁为铜”的记载(石胆是硫酸铜).这一方法开创了人类文明史上湿法冶金的先河.其中涉及到的化学反应类型是( )| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
分析 石胆能化铁为铜,可知发生CuSO4+Fe=FeSO4+Cu,以此来解答.
解答 解:石胆能化铁为铜,可知发生CuSO4+Fe=FeSO4+Cu,
A.生成物有两种,不属于化合反应,故A不选;
B.反应物有两种,不属于分解反应,故B不选;
C.为单质、化合物反应生成新单质、化合物的反应,属于置换反应,故C选;
D.反应物、生成物均有单质,不属于复分解反应,故D不选;
故选C.
点评 本题考查物质的性质及反应,为高频考点,把握习题中的信息、发生的反应、反应分类为解答的关键,侧重分析与应用能力的考查,注意金属活动性的应用,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
2.下列说法中不正确的是( )
| A. | 鉴定蔗糖水解产物中有葡萄糖:直接在水解液中加入新制Cu(OH)2悬浊液 | |
| B. | 鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可用灼烧的方法 | |
| C. | 乙醇可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化成乙酸 | |
| D. | 醇CH3CHOHCH3能在铜或银作催化剂的条件下发生催化氧化反应 |
19.关于如图所示装置的叙述,错误的是( )
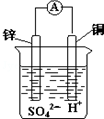

| A. | 电子从锌片经导线流向铜片 | B. | 氢离子在铜表面被还原,产生气泡 | ||
| C. | 锌是负极,其质量逐渐减小 | D. | 溶液由无色变为蓝色 |
6.为确定某溶液的离子组成,进行如下实验:
①取少量人员加Ba(NO3)2溶液,产生白色沉淀;
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体,白色沉淀部分溶解的气体;
③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验,以下推测不正确的是( )
①取少量人员加Ba(NO3)2溶液,产生白色沉淀;
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体,白色沉淀部分溶解的气体;
③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验,以下推测不正确的是( )
| A. | 一定有SO${\;}_{4}^{2-}$- | B. | 一定有CO32- | ||
| C. | 不能确定Cl-是否存在 | D. | 不能确定HCO3-是否存在 |
16.在100mL浓度为1mol/L的NaOH溶液中,通入1.68L SO2 气体(标况)后,在溶液中存在的溶质是( )
| A. | Na2SO3 和NaHSO3 | B. | Na2SO3 和NaOH | C. | Na2SO3 | D. | NaHSO4 |
3.在固定体积的容器中进行以下可逆反应:N2 (g)+3H2 (g)?2NH3 (g),能表明反应达平衡状态的是( )
| A. | 容器内气体压强不再改变 | |
| B. | 有2mol NH3生成的同时有3mol H2反应 | |
| C. | 生成NH3的量与反应掉N2的量之比为2:1 | |
| D. | N2、H2、NH3的物质的量之比为1:3:2 |
20.下列各反应属于取代反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| B. | CH2═CH2+Br2-→CH2BrCH2Br | |
| C. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O |
1.下列操作中正确的是( )
| A. | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL | |
| B. | 用托盘天平称取5.56 g KCl固体 | |
| C. | 配制450 mL 0.2 mol/L H2SO4溶液时应选用500 mL容量瓶 | |
| D. | 分液漏斗使用前需检查是否漏水,分液结束后漏斗中的上层液体从下口放出 |
