题目内容
19.关于如图所示装置的叙述,错误的是( )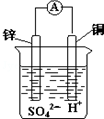
| A. | 电子从锌片经导线流向铜片 | B. | 氢离子在铜表面被还原,产生气泡 | ||
| C. | 锌是负极,其质量逐渐减小 | D. | 溶液由无色变为蓝色 |
分析 该装置是原电池,活泼金属锌作负极,铜作正极,负极上失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,以此解答该题.
解答 解:A.该原电池中,锌片是负极,电子从负极(锌片)经导线流向正极(铜片),故A正确;
B.正极铜上,氢离子得电子发生还原反应而生成氢气,故B正确;
C.锌为负极,失电子产生锌离子,锌离子进入溶液,所以锌质量逐渐减少,故C正确;
D.溶液中产生锌离子,锌离子在溶液中无色,正极铜不参加反应,溶液不可能变成蓝色,故D错误.
故选D.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,难度不大,注意把握电子、电流的流向,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.关于如图所示的装置叙述正确的是( )
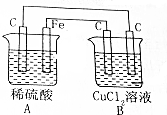

| A. | 装置A是电解池,装置B是原电池 | |
| B. | 装置A是原电池,装置B是电解池 | |
| C. | 电子由装置A中碳棒流向装置B中碳棒 | |
| D. | 工作一段时间后,A装置中稀H2SO4溶液质量减轻,B装置中CuCl2质量减轻 |
11.东汉成书的《神农本草经》有“石胆能化铁为铜”的记载(石胆是硫酸铜).这一方法开创了人类文明史上湿法冶金的先河.其中涉及到的化学反应类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
8.关于分液漏斗的使用,下列说法正确的是( )
| A. | 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质 | |
| B. | 分液漏斗在使用前只需检查旋塞芯处是否漏水即可 | |
| C. | 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁 | |
| D. | 放出下层液体后,再从漏斗下端口放出上层液体. |
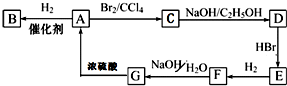 图中A~G均为有机化合物,根据图中的转化关系(反应条件略去),回答下列问题:
图中A~G均为有机化合物,根据图中的转化关系(反应条件略去),回答下列问题:
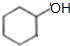 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O反应类型是消去反应.由F生成G的化学方程式
+H2O反应类型是消去反应.由F生成G的化学方程式 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +2H2O.
+2H2O.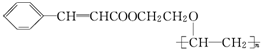
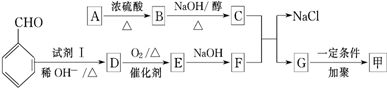
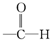 +
+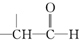 $→_{△}^{稀OH-}$
$→_{△}^{稀OH-}$ +H2O
+H2O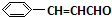 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2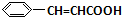 +H2O;③C与F的反应:
+H2O;③C与F的反应: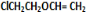 +
+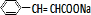 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$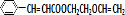 +NaCl.
+NaCl.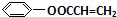 .
.