题目内容
4.从蛋白质水解产物中分离出一种氨基酸,经分析分子中只含有1个氮原子.0.19g此种氨基酸完全燃烧生成15.95mL N2(标准状况),求该氨基酸的含氮量和相对分子质量.若19.95g该氨基酸恰好和100mL 1.5mol•L-1 Ba(OH)2溶液中和,试写出其结构简式.分析 先求出氮气的质量,再求出质量分数,根据含有1个N原子求相对分子质量;根据氨基酸的物质的量和氢氧根物质的量求出羧基的数量,然后根据分子量得出结构.
解答 解:氮气的物质的量=$\frac{0.01595L}{22.4L/mol}$,质量为$\frac{0.01595L}{22.4L/mol}$×28g/mol=0.02g,质量分数为$\frac{0.02g}{0.19g}×100%$=10.5%,相对分子质量为$\frac{14}{10.5%}$=133;
19.95g该氨基酸的物质的量为$\frac{19.95g}{133g/mol}$=0.15mol,100ml 1.5mol/L的Ba(OH)2溶液的物质的量=0.15mol,故该氨基酸中含有2个羧基,还含有一个氨基,该氨基酸的结构简式为HOOC-CH(NH2)CH2-COOH,
答:该氨基酸的含氮量为10.5%,相对分子质量为133,结构简式为HOOC-CH(NH2)CH2-COOH.
点评 本题考查质量分数和相对分子质量的计算以及物质结构的推断,难度中等,注意先判断官能团的个数,然后确定结构.

练习册系列答案
相关题目
15.下列说法中正确的是( )
| A. | 在0℃、1.01×105Pa的条件下,某气体的体积约为2.24×10-2m3,该气体的物质的量为1 mol | |
| B. | 标准状况下,相同体积的任何气体单质所含的原子数相同 | |
| C. | 在20℃的温度下,1 mol某气体的体积约为22.4 L,该气体的压强为101 kPa | |
| D. | 固态的二氧化碳又叫干冰,含CO21 mol的干冰在标准状况下的体积必定小于22.4 L |
16.下列叙述正确的是( )
| A. | Na2O2可作供氧剂,而Na2O不行 | |
| B. | 钠在常温下不容易被氧化 | |
| C. | Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 | |
| D. | 钠在氯气中燃烧,生成白色的烟雾 |
13.下列配制溶液的操作能引起浓度偏高的是( )
| A. | 用1g 98%的浓硫酸加入4g水配制1:4硫酸溶液 | |
| B. | 配制2.0mo1•L-1硫酸溶液时,最后在容量瓶中加水稀释到标线,塞好盖子倒转摇匀后,发现液面低于标线 | |
| C. | 在100mL无水乙醇中,加人2g甲醛配制2%的甲醛洒精溶液 | |
| D. | 在80mL水中,加入18.4mol•L-1浓硫酸20mL,配制3.68mol•L-1稀硫酸 |
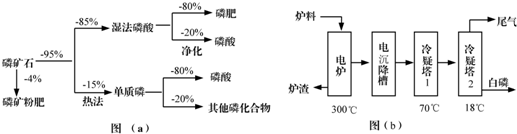
18.磷矿石主要以磷酸钙[Ca3(PO4)2•H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
部分物质的相关性质如下:
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的69%;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应化学方程式为:Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸0.49t.
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷.炉渣的主要成分是CaSiO3(填化学式).冷凝塔1的主要沉积物是液态白磷,冷凝塔2的主要沉积物是固态白磷.
(4)尾气中主要含有SiF4、CO,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去SiF4、H2S、HF;再通入次氯酸钠溶液,可除去PH3.(均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是产品纯度高.

部分物质的相关性质如下:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的69%;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应化学方程式为:Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸0.49t.
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷.炉渣的主要成分是CaSiO3(填化学式).冷凝塔1的主要沉积物是液态白磷,冷凝塔2的主要沉积物是固态白磷.
(4)尾气中主要含有SiF4、CO,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去SiF4、H2S、HF;再通入次氯酸钠溶液,可除去PH3.(均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是产品纯度高.