题目内容
12.己知ag的甲烷中含的b个H 原子,则阿佛加德罗常数为$\frac{4b}{a}$mol-1.分析 根据n=$\frac{m}{M}$计算出ag的甲烷的物质的量,然后计算出含有H原子的物质的量,最后根据阿伏伽德罗常数的计算表达式NA=$\frac{N}{n}$计算出阿伏伽德罗常数.
解答 解:ag的甲烷的物质的量为:n=$\frac{ag}{16g/mol}$=$\frac{a}{16}$mol,含有H原子的物质的量$\frac{a}{4}$,则阿伏伽德罗常数为:NA=$\frac{N}{n}$=$\frac{b}{\frac{a}{4}}$=$\frac{4b}{a}$,故答案为:$\frac{4b}{a}$.
点评 本题考查了阿伏伽德罗常数的计算,题目难度中等,明确阿伏伽德罗常数的概念及表达式即可解答,注意熟练掌握物质的量与摩尔质量、阿伏伽德罗常数等物理量之间的转化关系.

练习册系列答案
相关题目
3.在一定条件下,下列药物的主要成分都能发生四种反应的是( )
①取代反应 ②加成反应③水解反应 ④中和.
①取代反应 ②加成反应③水解反应 ④中和.
| A. | 维生素B5: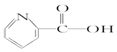 | B. | 阿司匹林: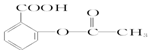 | ||
| C. | 芬必得: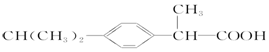 | D. | 摇头丸: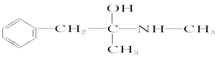 |
7.人民币一硬币有明亮的银白色的光泽且密度较大,小明同学认为一元硬币中含有铁,他这一想法属于科学探究过程的( )
| A. | 提出问题 | B. | 获得结论 | C. | 猜想 | D. | 反思 |
1.下列各组物质相互混合后,既有气体生成又有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中②过量的NaOH溶液和铝铵矾[NH4Al(SO4)2]溶液混合 ③少量电石(CaC2)投入到过量的NaHCO3溶液中④Na2O2投入到FeCl2溶液中.
①金属钠投入到FeCl3溶液中②过量的NaOH溶液和铝铵矾[NH4Al(SO4)2]溶液混合 ③少量电石(CaC2)投入到过量的NaHCO3溶液中④Na2O2投入到FeCl2溶液中.
| A. | ②④ | B. | ③ | C. | ②③ | D. | ①④ |
6.下列说法中,正确的是( )
| A. | 反应是放热反应还是吸热反应,由生成物与反应物的焓值差决定 | |
| B. | 升高温度,可以改变化学反应的反应热 | |
| C. | △H的大小与热化学方程式中的化学计量数无关 | |
| D. | 1 mol H2在足量Cl2中完全燃烧所放出的热量,是H2的燃烧热 |

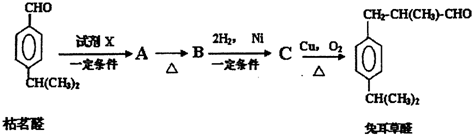

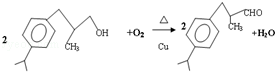 .
. 、
、 .
.