题目内容
1.下列反应属氧化还原反应,而水既不是氧化剂也不是还原剂的是( )| A. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | 2NO2+H2O═2HNO3+NO | D. | 2F2+2H2O═4HF+O2 |
分析 含元素化合价变化的反应为氧化还原反应,且水中H、O元素的化合价不变,则水既不是氧化剂也不是还原剂,以此来解答.
解答 解:A.不含元素的化合价变化,为非氧化还原反应,故A不选;
B.水中H元素的化合价降低,水为氧化剂,故B不选;
C.只有N元素的化合价变化,为氧化还原反应,而水既不是氧化剂也不是还原剂,故C选;
D.水中O元素的化合价升高,水为还原剂,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
15.NA为阿伏加德罗常数,下列物质所含原子数最多的是( )
| A. | 0.8molCO2 | B. | 标准状况下22.4LO2 | ||
| C. | 3.6g水 | D. | 含NA个NH3分子的氨气 |
16.水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O.下列说法中正确的是( )
| A. | 2molFe2+被氧化时有1molO2被还原 | B. | 该反应中只有Fe2+是还原剂 | ||
| C. | 每生成1molFe3O4转移2mol电子 | D. | 反应方程式中化学计量数x=2 |
6.实验室有下列试剂,其中必须用带橡胶塞的试剂瓶保存的是( )
①NaOH溶液 ②水玻璃 ③Na2S溶液 ④Na2CO3溶液 ⑤NH4Cl溶液 ⑥澄清石灰水 ⑦浓HNO3⑧浓H2SO4.
①NaOH溶液 ②水玻璃 ③Na2S溶液 ④Na2CO3溶液 ⑤NH4Cl溶液 ⑥澄清石灰水 ⑦浓HNO3⑧浓H2SO4.
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥⑦⑧ | D. | ⑤⑦⑧ |
13.科学家研制出了一种新型的贮氢材料-.这种镁铝合金的成分可表示为Mg17Al12.其贮氢和释氢的原理可表示为:Mg17Al12+17H2$?_{释氢}^{储氢}$17MgH2+12Al,下列有关说法正确的是( )
| A. | Mg17Al12是离子化合物 | |
| B. | 为防止金属氧化,熔炼制备Mg17Al12时通氮气做保护气 | |
| C. | 732 g的合金能吸收380.8 L氢气 | |
| D. | 该合金的熔点比镁和铝的熔点低 |
10. 已知反应:CO(g)+3H2(g)?CH4(g)+H2O(g).起始以物质的量之比为1:1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲).下列有关说法正确的是( )
已知反应:CO(g)+3H2(g)?CH4(g)+H2O(g).起始以物质的量之比为1:1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲).下列有关说法正确的是( )
 已知反应:CO(g)+3H2(g)?CH4(g)+H2O(g).起始以物质的量之比为1:1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲).下列有关说法正确的是( )
已知反应:CO(g)+3H2(g)?CH4(g)+H2O(g).起始以物质的量之比为1:1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲).下列有关说法正确的是( )| A. | 上述反应的△H<0 | |
| B. | N点时的反应速率一定比M点快 | |
| C. | 降低温度,H2的转化率可达到100% | |
| D. | 工业用此法制取甲烷应采用更高的压强 |
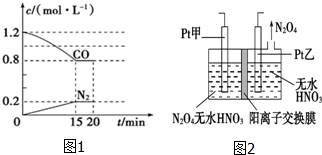 “霾”是当今世界环境热点话题.目前我国许多地方空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
“霾”是当今世界环境热点话题.目前我国许多地方空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应: 2015年8月12日天津港特大爆炸事故,再一次引发了人们对环境问题的关注.据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN).
2015年8月12日天津港特大爆炸事故,再一次引发了人们对环境问题的关注.据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN).