题目内容
7.下列反应的离子方程式正确的是( )| A. | 向碳酸氢铵溶液中加入过量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 将少量二氧化碳通入水玻璃中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| D. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
分析 A.氢氧根离子过量,氨根离子、碳酸氢根离子都发生反应;
B.原子个数不守恒;
C.将少量二氧化碳通入水玻璃中反应生成碳酸钠和硅酸沉淀;
D.次氯酸为弱电解质,应保留化学式.
解答 解:A.向碳酸氢铵溶液中加入过量的氢氧化钠溶液,离子方程式:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故A错误;
B.钠投入水中,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.将少量二氧化碳通入水玻璃中,离子方程式:CO2+SiO32-+H2O═CO32-+H2SiO3↓,故C正确;
D.氯气通入水中,离子方程式:Cl2+H2O═H++Cl-+HClO,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分、原子个数守恒,题目难度不大.

练习册系列答案
相关题目
17.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、[Al(OH)4]? | |
| B. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| C. | 中性溶液中可能大量存在Fe3+、K+、Cl?、SCN? | |
| D. | 加入铝粉能放出氢气的溶液中能大量存在K+、Ba2+、Cl-、Br- |
15.下列叙述正确的是:( )
①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂
②蛋白质遇酒精会变性,医疗中用99%的乙醇溶液进行消毒
③光导纤维的主要成分是二氧化硅
④氢氧化铁胶体具有杀菌净水作用
⑤碳酸钠、氢氧化钠、碳酸氢钠等都可以中和酸,故都可以作为治疗胃酸过多的药物
⑥可以用二氧化硅和水反应制备硅酸胶体.
①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂
②蛋白质遇酒精会变性,医疗中用99%的乙醇溶液进行消毒
③光导纤维的主要成分是二氧化硅
④氢氧化铁胶体具有杀菌净水作用
⑤碳酸钠、氢氧化钠、碳酸氢钠等都可以中和酸,故都可以作为治疗胃酸过多的药物
⑥可以用二氧化硅和水反应制备硅酸胶体.
| A. | ②③④ | B. | ①③ | C. | ①②④ | D. | ①③⑥ |
2.下列关于各实验装置图的叙述中,正确的是( )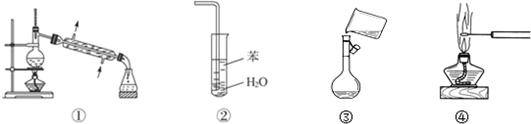

| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收NH3,并防止倒吸 | |
| C. | 图③是将溶解好的溶液转移到容量瓶中 | |
| D. | 图④可观察NaCl的焰色反应 |
12.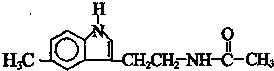 脑白金可以调整人体生物节律,达到改善睡眠的作用,是一种良好的保健品.脑白金主要成分的结构简式如图所示,下列对脑白金主要成分的推论正确的是( )
脑白金可以调整人体生物节律,达到改善睡眠的作用,是一种良好的保健品.脑白金主要成分的结构简式如图所示,下列对脑白金主要成分的推论正确的是( )
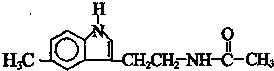 脑白金可以调整人体生物节律,达到改善睡眠的作用,是一种良好的保健品.脑白金主要成分的结构简式如图所示,下列对脑白金主要成分的推论正确的是( )
脑白金可以调整人体生物节律,达到改善睡眠的作用,是一种良好的保健品.脑白金主要成分的结构简式如图所示,下列对脑白金主要成分的推论正确的是( )| A. | 该物质有苯环属于芳香烃,1mol该物质能与5molH2加成 | |
| B. | 其分子式为C13H15N2O | |
| C. | 该物质不能与溴水反应 | |
| D. | 该物质能发生水解反应并生成乙酸 |
19.有钠、镁、铝各n mol,分别与等体积、均与含xmolHCl的盐酸反应,下列说法不正确的是( )
| A. | x<n时,钠生成的氢气最多 | B. | x=n时,钠、镁、铝生成的氢气一样多 | ||
| C. | n<x≤2n时,生成的氢气钠<镁=铝 | D. | x≥2n时,生成的氢气钠<镁<铝 |
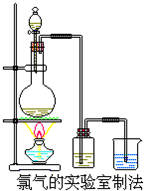 某校化学兴趣小组利用在加热条件下浓盐酸与二氧化锰的反应来制取并收集氯气,实验装置如图所示.
某校化学兴趣小组利用在加热条件下浓盐酸与二氧化锰的反应来制取并收集氯气,实验装置如图所示.