题目内容
2.下列关于各实验装置图的叙述中,正确的是( )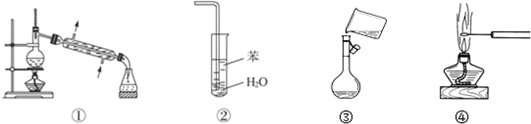
| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收NH3,并防止倒吸 | |
| C. | 图③是将溶解好的溶液转移到容量瓶中 | |
| D. | 图④可观察NaCl的焰色反应 |
分析 A.分离互不相溶的液体采用分液方法分离,分离互溶的液体采用蒸馏方法;
B.有缓冲作用的装置能防止倒吸;
C.配制一定物质的量浓度溶液时,转移溶液需要玻璃棒引流;
D.钠元素焰色反应呈黄色.
解答 解:A.分离互不相溶的液体采用分液方法分离,分离互溶的液体采用蒸馏方法,所以装置①常用于分离互溶的液体混合物,故A错误;
B.有缓冲作用的装置能防止倒吸,该装置没有缓冲作用,所以不能防倒吸,可以将苯换为四氯化碳溶液,故B错误;
C.配制一定物质的量浓度溶液时,转移溶液需要玻璃棒引流,否则易溅出液体导致配制溶液浓度偏低,故C错误;
D.钠元素焰色反应呈黄色,灼烧时直接观察即可,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及焰色反应、溶液配制、尾气处理、物质分离和提纯等知识点,侧重考查基本操作,明确实验原理及操作规范性即可解答,知道常见有缓冲作用的装置,题目难度不大.

练习册系列答案
相关题目
12. 已知在举国欢庆新中国60华诞之际,北京大街小巷对大量盆栽鲜花施用了S-诱抗素剂,以保证鲜花盛开,S-诱抗素的分子结构如图所示,下列关于该分子的说法正确的是( )
已知在举国欢庆新中国60华诞之际,北京大街小巷对大量盆栽鲜花施用了S-诱抗素剂,以保证鲜花盛开,S-诱抗素的分子结构如图所示,下列关于该分子的说法正确的是( )
 已知在举国欢庆新中国60华诞之际,北京大街小巷对大量盆栽鲜花施用了S-诱抗素剂,以保证鲜花盛开,S-诱抗素的分子结构如图所示,下列关于该分子的说法正确的是( )
已知在举国欢庆新中国60华诞之际,北京大街小巷对大量盆栽鲜花施用了S-诱抗素剂,以保证鲜花盛开,S-诱抗素的分子结构如图所示,下列关于该分子的说法正确的是( )| A. | S-诱抗素含有碳碳双键、羟基、羰基、羧基 | |
| B. | S-诱抗素分子式为C16H18O2 | |
| C. | S-诱抗素能发生加成反应、水解反应、氧化反应 | |
| D. | 1mol S-诱抗素在一定条件下可分别与4mol H2、2mol NaOH发生反应 |
13.下列说法中正确的是( )
| A. | 在分子中,两个成键的原子间的距离叫键长 | |
| B. | H-Cl键比H-I键稳定 | |
| C. | 含有极性键的一定是极性分子 | |
| D. | 键能越大,说明该分子越易受热分解 |
10.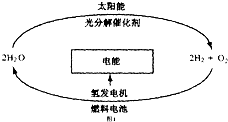 能源在各个方面的重要作用,科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法错误的是( )
能源在各个方面的重要作用,科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法错误的是( )
 能源在各个方面的重要作用,科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法错误的是( )
能源在各个方面的重要作用,科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法错误的是( )| A. | 在氢能的利用过程中,H2O可循环使用 | |
| B. | 开发和利用“氢能”,减少煤炭等化石能源的使用有助于控制臭氧空洞的形成 | |
| C. | 该法制氢的关键是寻找光分解催化剂 | |
| D. | 利用光电转化可将太阳能转化为电能用于电解水而获得氢气 |
17.下列离子方程式中书写正确的是( )
| A. | NaAlO2溶液滴入NaHCO3中:H++AlO2-+H2O=Al(OH)3↓ | |
| B. | 向FeI2溶液中滴加少量氯水:2Fe2++Cl2=2Fe3++2Cl- | |
| C. | 将2.24g铁粉投入400mL 0.3 mol/L的稀HNO3中:4Fe+12H++3NO3-=Fe3++3Fe2++3NO↑+6 H2O | |
| D. | 向含0.5 mol的明矾溶液中逐滴加入0.9 mol Ba(OH)2:5Al3++9SO42-+9Ba2++15OH-=9BaSO4↓+5Al(OH)3↓ |
7.下列反应的离子方程式正确的是( )
| A. | 向碳酸氢铵溶液中加入过量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 将少量二氧化碳通入水玻璃中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| D. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
14.下列有关性质的比较中,正确的是( )
| A. | 热稳定性:H2S>HCl>HBr>HI | B. | 熔点:Na2O>MgO>CaO | ||
| C. | 微粒半径:F-<Na+<Mg2+ | D. | 还原性:H2S>HCl>HF |
6.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2S | D. | NH3 H2O CO2 |