题目内容
5.研究CO2的利用对促进低碳社会的构建具有重要意义.(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.
己知:①Fe2O3(s)+3C(s,石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ/mol
②C(s,石墨)+CO2(g)=2CO(g)△H2=+172.5kJ/mol
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1.
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H<(填“>”、“<”或“=”,下同)0.
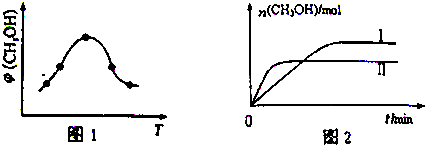
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、II对应的平衡常数关系为KI>KII.
(3)以CO2为原料还可以合成多种物质.工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,开始以氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为40%.
分析 (1)根据盖斯定律构造目标热化学方程式计算反应热;
(2)①平衡常数等于生成物的浓度系数次幂之积除以反应物浓度系数次幂之积;
②根据温度对平衡移动的影响判断反应热的符号;
③曲线Ⅱ到达平衡所用时间较短,则该条件下温度高,升高温度平衡逆移;
(3)根据反应物、反应条件、生成物写出化学反应式,然后利用三段式法计算.
解答 解:(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1
依据盖斯定律,①-②×3得Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g),故△H=489.0kJmol-1-3×172.5kJmol-1=-28.5kJmol-1,
故答案为:Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1;
(2)①二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),其平衡常数为:K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$,
故答案为:$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$;
②根据图象可知达到平衡后,温度越高,甲醇的体积分数φ(CH3OH)越小,说明升高温度平衡逆移,则正反应方向为放热反应,则△H<0,
故答案为:<;
③根据图象可知曲线Ⅱ到达平衡所用时间较短,则该条件下温度高,升高温度平衡逆移,平衡常数减小,则曲线Ⅱ条件下平衡常数较小,即KⅠ>KⅡ;
故答案为:>;
(3)根据反应物是二氧化碳和氨气(NH3),反应条件是高温、高压,生成物是尿素[CO(NH2)2]和水,化学反应式为:2NH3+CO2?CO(NH2)2+H2O,
设CO2的初始物质的量为a,则NH3的初始物质的量为3a,
2NH3+CO2?CO(NH2)2+H2O
起始/mol 3a a
转化/mol 1.2a 0.6a
平衡/mol 1.8a 0.4a
平衡时NH3转化率为:$\frac{1.2a}{3a}$×100%=40%,
故答案为:40%.
点评 本题考查了化学平衡的计算、盖斯定律的应用等知识,题目难度中等,明确化学平衡及其影响为解答关键,注意掌握盖斯定律的内容及应用方法,试题培养了学生的分析能力及化学计算能力.


| A. | 该反应的△H>0 | B. | 达平衡时,3v(H2)正=v(CO2)逆 | ||
| C. | a点对应的H2的平衡转化率为90% | D. | b点对应的平衡常数K值大于c点 |
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(2)250s时,H2的转化率为30%.
(3)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化92 kJ.下图能正确表示该反应中能量变化的是A.
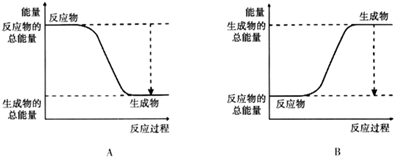
(4)为加快反应速率,可以采取的措施b
a.降低温度 b.增大压强 c.恒容时充入He气d.恒压时充入He气 e.及时分离NH3
(5)下列说法错误的是d
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.为了提高N2的转化率,应适当提高H2的浓度
d.250~350s生成物浓度保持不变,反应停止.
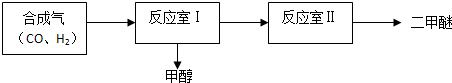
反应室Ⅰ:CO(g)+2H2(g)═CH3OH(g)
反应室Ⅱ:2CH3OH(g)═CH3OCH3(g)+H2O(g)
(1)欲提高反应室Ⅰ中CO的转化率,可以采取的方法有增大氢气浓度、不断分离出甲醇或者加压.
(2)反应室Ⅰ(恒容10L)中有关反应数据如下:
| 序号 | 温度(°C) | 起始浓度(mol•L-1) | 平衡浓度(mol•L-1) | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | ||
| ① | T | 1 | 3 | 0 | 0.2 | 1.4 | 0.8 |
| ② | T | 1.5 | 4.6 | 0.1 | b1 | b2 | b3 |
| ③ | T+30 | 1 | 3 | 0 | 0.25 | 1.5 | 0.75 |
②判断:$\frac{{b}_{3}}{{b}_{1}}$>4(填“>”、“<”或“=”).
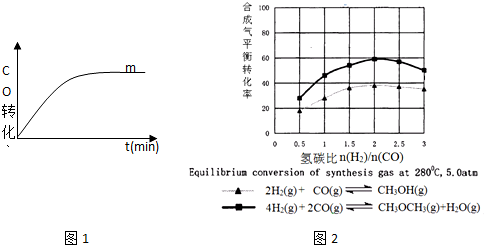
(3)图2表示甲醇或二甲醚体积分数随氢碳比$\frac{n({H}^{2})}{n(CO)}$的变化情况,从图中可以得到的结论是C.
A.提高氢碳比可以加快反应速率
B.提高氢碳比可以提高氢气的转化率
C.按方程式系数比投料时甲醇或二甲醚体积分数最大
D.对于同一反应氢碳比越大,生成物浓度越大
(4)已知某温度下下列热化学方程式:CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-20.59kJ•mol-1,则2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H3=-221.51kJ•mol-1.
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | Na2O+H2O=2NaOH | ||
| C. | Na2CO3+2HCl=2NaCl+H2O+CO2↑ | D. | 4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O |