题目内容
13.9g平均相对分子质量为26.2的CO和氢气组成的混合气体与足量氧气充分混合后,充分燃烧,立即通入足量的Na2O2固体中,固体增加的质量为多少克?
考点:有关混合物反应的计算
专题:计算题
分析:利用差量法,根据化学方程式分析:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.
2CO+O2
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2═2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2═4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
2CO+O2
| ||
2H2+O2
| ||
解答:
解:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.2CO+O2
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2═2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2═4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
所以13.9gCO和H2的混合气体在足量氧气中充分燃烧后,将产物立即通入盛有足量Na2O2的反应管,固体质量增重等于CO和H2的混合气体的质量为13.9g
答:固体质量增加13.9g.
| ||
2H2+O2
| ||
所以13.9gCO和H2的混合气体在足量氧气中充分燃烧后,将产物立即通入盛有足量Na2O2的反应管,固体质量增重等于CO和H2的混合气体的质量为13.9g
答:固体质量增加13.9g.
点评:本题考查混合物的计算,难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化分析规律,是解答该题的关键,避免计算的繁琐,侧重对学生思维能力的考查.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀逐渐溶解成深蓝色溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀,将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色.根据实验现象推测,下列描述中正确的是( )
| A、蓝色沉淀为Cu(OH)2,深蓝色溶液中所含Cu2+浓度较大 |
| B、白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应 |
| C、白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下发生了氧化还原反应 |
| D、反应过程中消耗的SO2与生成的SO2的物相等 |
能正确表示下列反应的离子方程式是( )
| A、Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| B、NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| C、向澄清石灰水中通入少量CO2:OH-+CO2═HCO3- |
| D、将0.2 mol?L-1的NH4Al(SO4)2溶液与0.3 mol?L-1的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、一定温度下,pH=6的纯水中含有OH-的数目为10-6 NA |
| B、120 g NaHSO4固体中含有的离子总数为2NA |
| C、标准状况下,22.4 L己烷中所含分子的数目为NA |
| D、100 mL 0.5 mol?L-1 的(NH4)2SO4 溶液中,NH4+的数目为 0.1 NA |
下列对化学知识概括合理的一组是( )
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③根据是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
④根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥氧化剂在反应中被氧化,还原剂在反应中被还原.
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③根据是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
④根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥氧化剂在反应中被氧化,还原剂在反应中被还原.
| A、只有①②③ | B、只有②③⑤ |
| C、只有③ | D、只有②④⑥ |
标况下由0.5g H2、11g CO和4g O2组成的混合气体,其体积约为( )
| A、8.4 L |
| B、11.2 L |
| C、14.0 L |
| D、16.8 L |
用NA表示阿伏加德罗常数,66克CO2所含的氧原子数为( )
| A、NA |
| B、2NA |
| C、3NA |
| D、4NA |
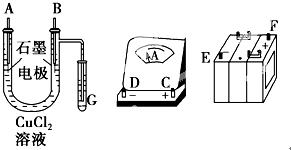 某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:
某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为: