题目内容
 已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)△H<0,如图中曲线a代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是( )
已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)△H<0,如图中曲线a代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是( )| A、增大A的浓度 |
| B、增大容器的体积 |
| C、加入催化剂 |
| D、升高温度 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应的特点是气体的计量数之和左右相等,且正反应放热,由图象可知a、b的反应速率不同,但达到同一平衡状态,以此解答该题.
解答:
解:在反应A(g)+2B(g)═3C(g)+D(s)中,气体反应物与气体生成物的化学计量数之和相等,则增大压强反应速率增大,但平衡不移动,由图象可知a、b的反应速率不同,但达到同一平衡状态,说明缩小容器的体积或加入催化剂都可实现图中转化,
故选C.
故选C.
点评:本题考查化学平衡的影响,侧重于学生的分析能力的考查,为高考常见题型,注意把握反应的特点以及图象曲线的变化趋势,为解答该题的关键,难度不大,答题时注意审题,把握题给信息.

练习册系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是( )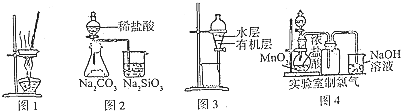

| A、用图l所示装置蒸干AlC13饱和溶液制备AlCl3晶体 |
| B、用图2所示装置证明非金属性Cl>C>Si |
| C、用图3所示装置分离CCl4萃取溴水后已分层的有机层和水层 |
| D、用图4所示装置制取少量Cl2气体 |
正确表示下列反应的离子方程式是( )
| A、碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
| B、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、硝酸铝溶液中加入过量氨水:Al3++NH3?H2O═AlO2-+4NH4++2H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓ |
将c(H+)=1×10-2mol?L-1的CH3COOH和HNO3溶液分别加水稀释100倍,稀释后两溶液的c(H+)分别为a和b.则a和b的关系为( )
| A、a>b | B、a=b |
| C、a<b | D、不能确定 |
 在一个固定容积的密闭容器中发生如下反应:
在一个固定容积的密闭容器中发生如下反应:N2 (g)+3H2 (g)
| △ |
在不同时间段里化学反应速率随时间变化如图所示,据此判断下列说法正确的是( )
| A、处于平衡状态的只有t1~t2段 |
| B、t1~t2段c(NH3)最大 |
| C、在t2时可能是向容器中充入了少量He |
| D、在t4时可能是升高温度 |
用铂作电极电解某金属氯化物MCln的水溶液,当阳极产生a mol气体时,阴极析出m g金属(无气体生成),则金属的相对原子质量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
将少量的CO2通入下列溶液中,没有沉淀产生的是( )
| A、Ba(OH)2溶液 |
| B、澄清石灰水 |
| C、氯化钡溶液 |
| D、漂白粉溶液 |