题目内容
已知硫酸镁固体和木炭在隔绝空气的情况下高温煅烧,可以发生如下以下反应:
2MgSO4+C
2MgO+2SO2↑+CO2↑、MgSO4+3C
MgO+S↑+3CO↑.
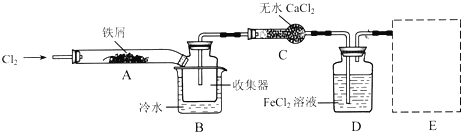
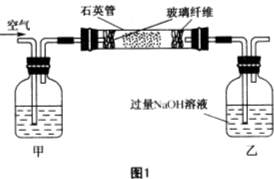
某同学利用如图装置对煅烧产生的混合气体进行成分检验、分步吸收或收集.请回答有关问题:
(1)高温时,MgSO4与木炭反应还可以同时生成SO2、CO两种还原性气体,写出该反应的化学方程式 .
(2)A中得到的淡黄色固体与热的NaOH溶液反应,产物中各元素价态最高为+4,写出该反应的离子方程式: .
(3)B、C两装置的作用分别是检验、吸收某一种气体,则B中盛放的溶液可以是 ,C 中盛放的溶液可以是 (均填序号).
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.Na2SO3 溶液 e.品红试液
(4)D中盛放澄清石灰水,能否根据“有白色沉淀生成”来判断混合气体中一定含有CO2?你的结论及其理由是 .
(5)E中盛放NaOH溶液,以保证F中收集到较纯净的CO(不计水的挥发).F中两种玻璃容器的名称分别是 .
2MgSO4+C
| ||
| ||
某同学利用如图装置对煅烧产生的混合气体进行成分检验、分步吸收或收集.请回答有关问题:

(1)高温时,MgSO4与木炭反应还可以同时生成SO2、CO两种还原性气体,写出该反应的化学方程式
(2)A中得到的淡黄色固体与热的NaOH溶液反应,产物中各元素价态最高为+4,写出该反应的离子方程式:
(3)B、C两装置的作用分别是检验、吸收某一种气体,则B中盛放的溶液可以是
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.Na2SO3 溶液 e.品红试液
(4)D中盛放澄清石灰水,能否根据“有白色沉淀生成”来判断混合气体中一定含有CO2?你的结论及其理由是
(5)E中盛放NaOH溶液,以保证F中收集到较纯净的CO(不计水的挥发).F中两种玻璃容器的名称分别是
考点:性质实验方案的设计
专题:实验设计题
分析:(1)根据题干信息:高温时,MgSO4与木炭反应还可以同时生成SO2、CO两种还原性气体来书写方程式;
(2)硫单质可以和氢氧化钠在加热下发生反应生成硫化钠、亚硫酸钠和水,据此书写离子方程式;
(3)检验二氧化硫用品红,再用亚硫酸钠吸收二氧化硫,然后确保二氧化硫吸收干净了,再进行二氧化碳的检验,一氧化碳可以用排水法收集;
(4)根据二氧化硫、二氧化碳都可以使石灰水变浑浊来解答;
(5)根据F装置中的仪器来回答判断.
(2)硫单质可以和氢氧化钠在加热下发生反应生成硫化钠、亚硫酸钠和水,据此书写离子方程式;
(3)检验二氧化硫用品红,再用亚硫酸钠吸收二氧化硫,然后确保二氧化硫吸收干净了,再进行二氧化碳的检验,一氧化碳可以用排水法收集;
(4)根据二氧化硫、二氧化碳都可以使石灰水变浑浊来解答;
(5)根据F装置中的仪器来回答判断.
解答:
解:(1)根据题干信息:高温时,MgSO4与木炭反应还可以同时生成SO2、CO两种还原性气体,得出方程式为:MgSO4+C
MgO+SO2↑+CO↑,故答案为:MgSO4+C
MgO+SO2↑+CO↑;
(2)硫单质可以和氢氧化钠在加热下发生反应生成硫化钠、亚硫酸钠和水,离子方程式为:3S+6OH-
2S2-+SO32-+3H2O,故答案为:3S+6OH-
2S2-+SO32-+3H2O;
(3)首先检验二氧化硫用品红,品红褪色,证明二氧化硫存在,再用亚硫酸钠吸收二氧化硫,不能用氢氧化钠吸收,否则,二氧化碳会无法检验,然后确保二氧化硫吸收干净了,再进行二氧化碳的检验,二氧化碳能使石灰水变浑浊,最后一氧化碳可以用排水法收集;
故答案为:e;d;
(4)D中盛放澄清石灰水,二氧化硫、二氧化碳都可以使石灰水变浑浊,所以不能根据“有白色沉淀生成”来判断混合气体中一定含有CO2,故答案为:不能,无法确定C装置已将SO2吸收完全;
(5)F装置是收集CO的装置,其中的玻璃仪器水槽、集气瓶,故答案为:水槽、集气瓶.
| ||
| ||
(2)硫单质可以和氢氧化钠在加热下发生反应生成硫化钠、亚硫酸钠和水,离子方程式为:3S+6OH-
| ||
| ||
(3)首先检验二氧化硫用品红,品红褪色,证明二氧化硫存在,再用亚硫酸钠吸收二氧化硫,不能用氢氧化钠吸收,否则,二氧化碳会无法检验,然后确保二氧化硫吸收干净了,再进行二氧化碳的检验,二氧化碳能使石灰水变浑浊,最后一氧化碳可以用排水法收集;
故答案为:e;d;
(4)D中盛放澄清石灰水,二氧化硫、二氧化碳都可以使石灰水变浑浊,所以不能根据“有白色沉淀生成”来判断混合气体中一定含有CO2,故答案为:不能,无法确定C装置已将SO2吸收完全;
(5)F装置是收集CO的装置,其中的玻璃仪器水槽、集气瓶,故答案为:水槽、集气瓶.
点评:本题是一道物质的性质实验方案设计探究题,考查学生物质的性质、检验等知识,注意知识的灵活应用是关键,难度中等.

练习册系列答案
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
“群众利益无小事,食品安全是大事”.下列做法不会损害人体健康的是( )
| A、用干冰保藏易变质的食品 |
| B、用硫磺熏制白木耳、粉丝等食品 |
| C、用甲醛浸泡易腐烂的食品 |
| D、用含亚硝酸钠的工业用盐腌制食品 |
下列有关制取蒸馏水的装置和操作的说法中,不正确的是( )
| A、温度计的水银球应插入蒸馏烧瓶内的自来水中 |
| B、冷凝管内水的流向是下进上出 |
| C、实验中需在自来水中加几片碎瓷片 |
| D、蒸馏烧瓶底部必须垫石棉网 |
下列各组有机化合物中,肯定互为同系物的一组是( )
| A、C3H6与C5H10 |
| B、C4H6与C5H8 |
| C、C3H8与C5H12 |
| D、C2H2与C6H6 |

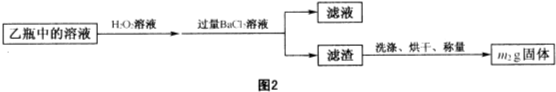
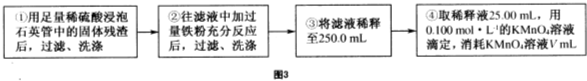
 黄铁矿(主要成分为FeS2,含少量其他金属硫化物)曾是我国一些硫酸厂制取硫酸够主要原料.某化学学习小组对黄铁矿石进行如下实验探究:
黄铁矿(主要成分为FeS2,含少量其他金属硫化物)曾是我国一些硫酸厂制取硫酸够主要原料.某化学学习小组对黄铁矿石进行如下实验探究: