题目内容
附加题
已知2X2(g)+Y2(g)?2Z(g)△H=-a kJ/mol(a>0),在一个容积固定的容器中加入2molX2和1molY2,在500℃时充分反应达平衡后,Z的浓度为W mol/l,放出热量b kJ.
①当此容器中起始加入X2 为1mol、Y2 为0.5mol、Z 为1mol时,反应达平衡后Z的浓度 W mol/l(填“>”、“<”或“=”).
②若原来容器中只加入2molZ,500℃充分反应达平衡后,吸收热量为C kJ,则Z的浓度 W mol/l(填“>”、“<”或“=”),a、b、c之间满足关系 用代数式表示)
③若此容器中起始加入X2 为6mol、Y2 为3mol时,反应达平衡后Z的体积分数将 (填“增大”、“减小”、“不变”)
④若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2达到平衡后.Y2的转化率将 (填“增大”、“减小”、“不变”)
已知2X2(g)+Y2(g)?2Z(g)△H=-a kJ/mol(a>0),在一个容积固定的容器中加入2molX2和1molY2,在500℃时充分反应达平衡后,Z的浓度为W mol/l,放出热量b kJ.
①当此容器中起始加入X2 为1mol、Y2 为0.5mol、Z 为1mol时,反应达平衡后Z的浓度
②若原来容器中只加入2molZ,500℃充分反应达平衡后,吸收热量为C kJ,则Z的浓度
③若此容器中起始加入X2 为6mol、Y2 为3mol时,反应达平衡后Z的体积分数将
④若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2达到平衡后.Y2的转化率将
考点:有关反应热的计算,化学平衡的影响因素,化学平衡的计算
专题:化学反应中的能量变化,化学平衡专题
分析:①恒温恒容下,1molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同;
②恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同;
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,根据反应热计算两个过程的热量数值,据此判断;
③恒容时,气体的物质的量越多,压强越大,平衡向右移,Z的体积分数增大;
④原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,据此判断.
②恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同;
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,根据反应热计算两个过程的热量数值,据此判断;
③恒容时,气体的物质的量越多,压强越大,平衡向右移,Z的体积分数增大;
④原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,据此判断.
解答:
解:①恒温恒容下,1molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=Wmol?L-1,故答案为:=;
②恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=Wmol?L-1,
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,
对于反应2X2(g)+Y2(g)?2Z(g)△H=-akJ?mol-1,则b=n×
,对于反应2Z(g)?2X2(g)+Y2(g)△H=akJ?mol-1,Z分解的物质的量为(2-n)mol,故c=
×a=1-n×
,故a=b+c,
故答案为:=;a=b+c;
③在一个容积固定的容器中加入6molX2和3molY2,由于气体的物质的量越多,压强越大,平衡向右移,故Z的体积分数增大,故答案为:增大;
④原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,即向正反应移动,Y2的转化率变大,故答案为:增大.
②恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=Wmol?L-1,
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,
对于反应2X2(g)+Y2(g)?2Z(g)△H=-akJ?mol-1,则b=n×
| a |
| 2 |
| 2-n |
| 2 |
| a |
| 2 |
故答案为:=;a=b+c;
③在一个容积固定的容器中加入6molX2和3molY2,由于气体的物质的量越多,压强越大,平衡向右移,故Z的体积分数增大,故答案为:增大;
④原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,即向正反应移动,Y2的转化率变大,故答案为:增大.
点评:本题考查化学平衡常数、平衡状态判断,化学平衡的有关计算等,注意(4)中构建平衡建立的途径,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
生活中处处有化学.下列说法正确的是( )
| A、煎炸食物的花生油和牛油都是可皂化的饱和酯类 |
| B、做衣服的棉和麻均与淀粉互为同分异构体 |
| C、制饭勺、饭盒、高压锅等的不锈钢是合金 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
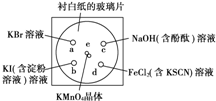 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol?L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,各种液滴彼此分开,围成半径小于表面皿的圆形(如图所示)在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol?L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,各种液滴彼此分开,围成半径小于表面皿的圆形(如图所示)在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.