题目内容
10.为了研究外界条件对H2O2分解速率的影响,有同学利用实验室提供的仪器和试剂设计了如下4组实验.注意:设计实验时,必须控制只有一个变量!试剂:4% H2O2溶液,12% H2O2溶液,lmol/LFeCl3溶液
仪器:试管、带刻度的胶头滴管、酒精灯
| 组别 | 实验温度 (℃) | H2O2溶液 | FeCl3溶液 (1mol/L) |
| 1 | 30 | 5mL 4% | 1mL |
| 2 | 60 | 5mL 4% | 1mL |
| 3 | 30 | 5mL 12% | |
| 4 | 30 | 5mL 4% |
(2)乙同学进行实验3与实验4,发现气体均缓慢产生,无法说明“浓度改变会影响化学反应速率”,你的改进方法是再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂.
(3)丙同学进行了实验1与实验4,你认为他想探究的是探究催化剂对化学反应速率的影响.该方案设计是否严谨?否(填是或否),说明理由试管中加入1mL1mol/LFeCl3溶液会使H2O2溶液的浓度降低.
分析 (1)通过比较表格中的数据的异同点进行解答,根据控制变量法来分析研究的对象;
(2)提供催化剂,加快反应速率,现象更为明显;
(3)实验3两试管中双氧水的浓度相同,有一支试管中加入了氯化铁溶液,氯化铁作催化剂,则可知实验3的目的;加入的1mL溶液会对乙试管溶液进行稀释,会使浓度发生改变.
解答 解:(1)实验1、2只有温度不同,所以研究的是温度对反应速率的影响,
故答案为:1、2;
2)向试管甲中加入5mL12%H2O2溶液,向试管乙中加入5mL4%H2O2溶液,再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂,加快反应速率,现象更为明显,故改进方法是再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂,
故答案为:再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂;
(3)只有一支试管中加入了氯化铁溶液,与另一支试管形成对比试验,则实验目的是探究催化剂对化学反应速率的影响;但此方案设计不合理,因为加入的1mL溶液会对试管溶液进行稀释,使浓度发生改变,
故答案为:探究催化剂对化学反应速率的影响;否;试管中加入1mL1mol/LFeCl3溶液会使H2O2溶液的浓度降低.
点评 本题考查了探究影响反应速率的因素,实验方案的设计,难度一般,注意试验过程中单一变量研究方法的使用,为易错点.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
8.下列实验设计正确的是( )
| A. | 检验淀粉已完全水解;在淀粉水解液中滴加碘水 | |
| B. | 证明氧化性H2O2比Fe3+强,将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | |
| C. | 检验某溶液中含Fe2+:可先向溶液中加入氯气,再滴加少量KSCN溶液 | |
| D. | 把0.9mol•L-1硫酸100mL;将18 mol•L-1硫酸5mL移入100mL容量瓶,加水至刻度 |
1.一种以2mol•L-1的Na2SO4溶液为电解质溶液的钠离子电池的总反应如下(P为+5价):NaTi2(PO4)3+Zn+Na2SO4$?_{充电}^{放电}$Na3Ti2(PO4)3+ZnSO4下列有关说法正确的是( )
| A. | 放电时,NaTi2(PO4)3发生氧化反应 | |
| B. | 放电时,Na+向锌棒一极移动 | |
| C. | 充电时,阳极反应式为[Ti2(PO4)3]+-2e-=[Ti2(PO4)3]3+ | |
| D. | 充电时,每转移0.2 mol电子,阴极增重6.5 g |
18.短周期主族元素W、X、Y、Z的原子序数依次增大,四种原子的最外层电子数之和为19.X原子的电子总数与最外层电子数之比为l:3,Y原子的最外层电子数与其内层电子总数之比为1:10.下列说法正确的是( )
| A. | 简单离子的半径:Y>X | |
| B. | 最简单气态氢化物的稳定性:W>X | |
| C. | 化合物WX、YZ中化学键类型相同 | |
| D. | W、Z的最高价氧化物对应的水化物均为强酸 |
5.CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色.实验室制备CuBr的反应原理为SO2+2CuSO4+2NaBr+2H2O═2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的是( )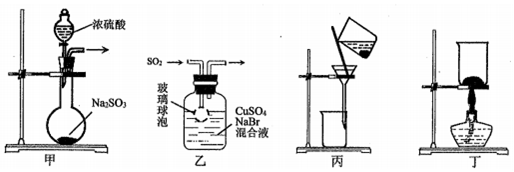

| A. | 用装置甲制取SO2 | B. | 用装置乙制取CuBr | ||
| C. | 用装置丙避光将CuBr与母液分离 | D. | 用装置丁干燥CuBr |
15.下列有关说法不正确的是( )
| A. | 反应SiO2(s)+3C(s)═SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H>0 | |
| B. | 等pH的CH3COOH、HCl溶液混合后,平衡不移动,但c(CH3COO-)减少 | |
| C. | 配制KF溶液时,必需要加入KOH溶液抑制F-水解 | |
| D. | 向NaHS溶液中滴入少量CuCl2溶液产生黑色沉淀,HS-电离程度增大,pH减小 |
2.某固定体积的密闭容器中,加入一定量的A达化学平衡:aA(g)?bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )
| A. | 若a=b+c时,B的物质的量分数变大 | B. | 若a=b+c时,B的体积分数不变 | ||
| C. | 若a>b+c时,A的转化率变小 | D. | 若a<b+c时,A的转化率变大 |
19.下列说法正确的是( )
| A. | SO2与SO3互为同分异构体 | |
| B. | 氢气是理想的绿色能源 | |
| C. | 单质中不存在化学键 | |
| D. | 电解饱和氯化钠溶液可能得到金属钠 |
20.下列关于化学反应限度的说法正确的是( )
| A. | 当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的限度 | |
| B. | 可以通过延长化学反应时间改变化学反应限度 | |
| C. | 平衡状态是一种静止的状态,因为反应物和生成物的浓度不再改变 | |
| D. | 化学反应的限度不可以通过改变条件而发生改变 |