题目内容
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、1mol O2与金属钠反应,O2不一定得到4NA个电子 |
| B、标准状况下,a L CH4和a L C6H14中所含分子数均为a NA/22.4 |
| C、常温常压下,1mol氯气与足量的金属镁反应,转移2NA个电子 |
| D、在20℃、1.01×105 Pa时,2.8g C2H4和CO的混合气体含气体分子数等于0.1 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1molO2与钠反应生成Na2O2时,得到2NA个电子;
B.标准状况下C6H14为液态;
C.氯元素化合价从0价降到-1价,所以Cl2~2Cl-~2e-;
D.C2H4和CO的分子量都是28,2.8g C2H4和CO的混合气体的物质的量为0.1mol.
B.标准状况下C6H14为液态;
C.氯元素化合价从0价降到-1价,所以Cl2~2Cl-~2e-;
D.C2H4和CO的分子量都是28,2.8g C2H4和CO的混合气体的物质的量为0.1mol.
解答:
解:A.当O2与钠反应生成Na2O2时,1mol O2只能得到2NA个电子,故A正确;
B.标准状况下C6H14为液态,无法计算物质的量,故B错误;
C.1mol氯气与足量的金属镁反应,氯元素化合价从0价降到-1价,所以Cl2~2Cl-~2e-,1mol氯气与足量的金属镁反应,转移2NA个电子,故C正确;
D.2.8g C2H4和CO的混合气体的物质的量为0.1mol,因此气体的分子数等于0.1 NA,故D正确.
故选B.
B.标准状况下C6H14为液态,无法计算物质的量,故B错误;
C.1mol氯气与足量的金属镁反应,氯元素化合价从0价降到-1价,所以Cl2~2Cl-~2e-,1mol氯气与足量的金属镁反应,转移2NA个电子,故C正确;
D.2.8g C2H4和CO的混合气体的物质的量为0.1mol,因此气体的分子数等于0.1 NA,故D正确.
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要是气体摩尔体积的应用条件,氧化还原反应的电子转移数的计算,质量与微粒数的计算关系,关键是钠与氧气反应时条件不同产物不同的分析,难度不大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
将等物质的量的甲烷与氯气在光照条件下反应,得到的产物最多的是( )
| A、HCl |
| B、CH2Cl2 |
| C、CH3Cl |
| D、CCl4 |
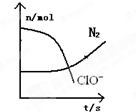 某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )| A、还原剂是CN-,氧化产物只有N2 |
| B、氧化剂是ClO-,还原产物是HCO3- |
| C、配平后氧化剂与还原剂的计量系数之比为5:2 |
| D、标准状况下若生成2.24LN2,则转移电子0.5 mol |
下列说法中,不正确的是( )
| A、硅单质常用于制造太阳能电池和光纤 |
| B、石灰石在工业上常用制造水泥和玻璃 |
| C、碳酸氢钠在医疗上可用于治疗胃酸过多 |
| D、氧化铝可用于制造耐高温的容器 |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
| B、标准状况下,11.2 L H2O 所含的分子数为0.5NA |
| C、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| D、18g H2O 和H2O2 的混合物含有的分子数为1NA |
短周期元素aW、bX、cY、dZ的原子序数依次增大,且b-a=d-c.aW、cY、dZ与bX 都能相成AB2型共价化合物,但晶体的类型不完全相同.下列叙述中不正确的是( )
| A、WZ2分子中所有原子最外层都为8电子结构 |
| B、WX2、ZX2的化学键类型和晶体类型都相同 |
| C、4种元素的气态氢化物中X的气态氢化物最稳定 |
| D、原子半径大小顺序为X<W<Y<Z |
关于O2与O3气体,下列比值一定为2:3的是( )
| A、若两种气体所占体积相同,两种气体的质量之比 |
| B、若两种气体原子数相同,两种气体的质子数之比 |
| C、若温度及压强相同,两种气体的密度之比 |
| D、若两种气体的质量相同,两种气体的分子数之比 |