题目内容
以下各分子中,所有原子都满足最外层为8电子结构的是( )
| A、H3O+ |
| B、BF3 |
| C、P4 |
| D、PCl5 |
考点:化学键,原子核外电子排布
专题:化学键与晶体结构
分析:根据原子最外层电子数和化合价判断,在化合物中,原子最外层电子数=原子的价层电子数+|化合价|,以此进行分析.
解答:
解:A.H3O+中含有氢原子,不满足8电子结构,故A错误;
B.BF3中B元素的化合价为+3,B原子最外层电子数为3,则3+3=6,故B原子不满足8电子结构,氯元素化合价为-1价,氯原子最外层电子数为7,则|-1|+7=8,故Cl原子满足8电子结构,故B错误;
C.白磷P4的结构式为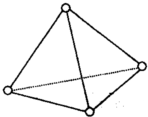 ,P原子最外层电子数是5,每个P原子形成3个共价键,所以白磷中P原子满足8电子结构,故C正确;
,P原子最外层电子数是5,每个P原子形成3个共价键,所以白磷中P原子满足8电子结构,故C正确;
D.PCl5中,P原子的最外层电子为:5+5=10,Cl原子的最外层电子为:7+|-1|=8,不都满足8电子稳定结构,故D错误;
故选C.
B.BF3中B元素的化合价为+3,B原子最外层电子数为3,则3+3=6,故B原子不满足8电子结构,氯元素化合价为-1价,氯原子最外层电子数为7,则|-1|+7=8,故Cl原子满足8电子结构,故B错误;
C.白磷P4的结构式为
 ,P原子最外层电子数是5,每个P原子形成3个共价键,所以白磷中P原子满足8电子结构,故C正确;
,P原子最外层电子数是5,每个P原子形成3个共价键,所以白磷中P原子满足8电子结构,故C正确;D.PCl5中,P原子的最外层电子为:5+5=10,Cl原子的最外层电子为:7+|-1|=8,不都满足8电子稳定结构,故D错误;
故选C.
点评:本题考查了8电子结构的判断,可以根据元素化合价的绝对值与其最外层电子数的和来分析解答,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
能与大量Fe3+共存的是( )
| A、Fe |
| B、S2- |
| C、Cu2+ |
| D、Cu |
下列物质中,不能和氯气发生取代反应的是( )
| A、CH3Cl |
| B、CCl4 |
| C、CH2Cl2 |
| D、CH4 |
把0.05molBa(OH)2固体分别加入到下列100mL液体中,溶液导电性基本不变.该液体是( )
| A、1.0mol/L盐酸 |
| B、自来水 |
| C、0.5mol/L硫酸 |
| D、1.0mol/L氨水 |
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:下列判断正确的是( )
| 实验编号 | 起始浓度/(mol?L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A、实验①反应后的溶液中:c(A-)>c(K+)>c(OH-)>c(H+) | ||
B、实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=
| ||
| C、实验②反应后的溶液中:c(A-)+c(HA)<0.1 mol/L | ||
| D、实验②反应后的溶液中:c(K+)+c(OH-)=c(H+)+c(A-) |
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)?3C(g),若反应开始时充入2molA和2molB,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数小于a%的是( )
| A、2molC |
| B、2 molA、1 molB和1 molHe(不参加反应) |
| C、1 molB和1 molC |
| D、2 molA、2 molB和3 molC |
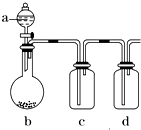 有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.
有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.