题目内容
已知NA代表阿伏加德罗常数,下列说法正确的是( )
| A、34 g H2O2中含有的阴离子数为NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、1mol重甲基(-CD3)含有电子数为9NA |
| D、1 mol铁铝混合物与足量稀盐酸反应时,转移电子数是3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.H2O2是共价化合物,分子中没有阴离子;
B.铝离子为强酸弱碱盐,部分铝离子发生水解;
C.1个C含有6个电子,1个D含有1个电子;
D.铁与稀盐酸反应生成二价铁离子.
B.铝离子为强酸弱碱盐,部分铝离子发生水解;
C.1个C含有6个电子,1个D含有1个电子;
D.铁与稀盐酸反应生成二价铁离子.
解答:
解:A.H2O2是共价化合物,分子中没有阴离子,故A错误;
B.铝离子为强酸弱碱盐,部分铝离子发生水解,所以在AlCl3溶液中,如果铝离子的个数为NA,则Cl-总数应大于3NA,故B错误;
C.1个C含有6个电子,1个D含有1个电子,1个重甲基(-CD3)含有9个电子,所以1mol重甲基(-CD3)含有电子数为9NA,故C正确;
D.铁与稀盐酸反应生成二价铁离子,1 mol铁铝混合物,不知道铁和铝的物质的量,无法确定失去电子总数,故D错误;
故选:C.
B.铝离子为强酸弱碱盐,部分铝离子发生水解,所以在AlCl3溶液中,如果铝离子的个数为NA,则Cl-总数应大于3NA,故B错误;
C.1个C含有6个电子,1个D含有1个电子,1个重甲基(-CD3)含有9个电子,所以1mol重甲基(-CD3)含有电子数为9NA,故C正确;
D.铁与稀盐酸反应生成二价铁离子,1 mol铁铝混合物,不知道铁和铝的物质的量,无法确定失去电子总数,故D错误;
故选:C.
点评:本题考查了阿伏伽德罗常数的应用,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的转化关系是解题关键,注意强酸弱碱盐在溶液中发生水解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、常温常压下,3.2 g O3所含电子数为1.2 NA |
| B、常温常压下,34g H2O2中含有质子的数目为34 NA |
| C、标准状况下,11.2 L CO与11.2 L O2混合所含原子数为2NA |
| D、0.1 mol CO32-,所含电子数为38NA |
向三份0.1mol?L-1CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、NaCl固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
| A、减小、增大、减小 |
| B、增大、减小、不变 |
| C、减小、增大、不变 |
| D、增大、减小、增大 |
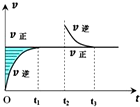 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中不正确的是( )| A、Z和W在该条件下一定不为气态 |
| B、t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C、若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D、若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
下列叙述不正确的是( )
| A、白铁(镀锌铁)镀层破损后,先被腐蚀的是铁 |
| B、锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率 |
| C、钢铁表面常易锈蚀生成Fe2O3?nH2O |
| D、金属的腐蚀主要是电化学腐蚀 |
对于下面的反应 14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
| A、氧化剂只有CuSO4 |
| B、Cu2S 既是氧化剂又是还原剂 |
| C、被氧化的硫与被还原的硫的质量比为3:7 |
| D、14mol CuSO4可氧化5mol FeS2 |
判断食物的酸碱性,是根据食物进入人体后所生成的最终代谢物的酸碱性而定.含氮、磷等非金属元素较多食物,为酸性食物;含钠、钾、钙、镁等金属元素食物较多,为碱性食物.对食物的酸、碱性判断正确的是
( )
( )
| A、苹果是酸性食物 |
| B、猪肉、牛肉是碱性食物 |
| C、大米、面包是碱性食物 |
| D、巧克力、奶油是酸性食物 |
 元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系:
元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系: