题目内容
10.下列说法中,正确的是( )| A. | 分子中键的极性越强,分子越稳定 | |
| B. | 若把H2S写成H3S,违背了共价键的饱和性 | |
| C. | 分子中共价键的键能越大,键越长,则分子越稳定 | |
| D. | 分子中共价键的键能越大,该物质的性质越不活泼 |
分析 A.分子的稳定性与键的强弱有关;
B.S最外层有6个电子,只能结合2个H;
C.键长越短,键能越大;
D.物质的活泼性不仅与键能有关,还与分子中各个键的空间分布有关.
解答 解:A.分子的稳定性与键的强弱有关,与键的极性无关,单质非极性分子中键的极性为零,分子也很稳定,如氮气,故A错误;
B.S最外层有6个电子,只能结合2个H,形成H2S分子,若写成H3S分子,违背了共价键的饱和性,故B正确;
C.一般分子中共价键的键能越大,键越越短,分子越稳定,故C错误;
D.物质的活泼性不仅与键能有关,还与分子中各个键的空间分布有关,分子活泼性是分子整体的性质,而一个分子并非只有一个化学键,故D错误.
故选B.
点评 本题考查共价键的形成、物质稳定性的影响因素等,把握共价键的方向性和饱和性为解答的关键,侧重分析与应用能力的考查,题目难度不大

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列说法中正确的是( )
| A. | Na2O2可作漂白剂和供氧剂,碳酸钠可用于治疗胃酸过多 | |
| B. | 工业上用次氯酸制漂白粉,保存漂白粉的塑料袋要密封 | |
| C. | 氯气用于自来水消毒,是因为生成的次氯酸有杀菌、消毒的作用 | |
| D. | 溴化银用于人工降雨,单质碘加入食盐中用于制加碘盐 |
7.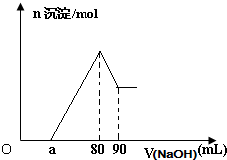 将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
 将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )
将一块镁铝合金投入一定体积的1mol/L稀盐酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积的关系如图.下列说法中不正确的是( )| A. | 由图可以确定该镁铝合金中铝的质量为0.27 g | |
| B. | 由图可以确定该合金中两元素的物质量之比的最大值为4 | |
| C. | 当滴入1mol/L的NaOH溶液85mL时,所得沉淀的成分为Mg(OH)2和Al(OH)3 | |
| D. | 由图可以确定a的取值范围为:0≤a≤50 |
4.关于分散系的说法,正确的是( )
| A. | 根据体系的稳定性,可将分散系分为溶液、胶体和浊液 | |
| B. | 一种分散系的分散质可以是固态、液态或气态,但只能是纯净物 | |
| C. | 利用丁达尔效应可以区分溶液和胶体,它利用了光的衍射原理 | |
| D. | 火力发电厂的烟气管道里安装的静电除尘装置,它利用了胶体的电泳原理 |
15.学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
找出上述三组分类中的错误,错误物质的化学式为Na2CO3、Al2O3.
(2)下列2个反应,按要求填写相关量.
①2Na2O2+2H2O=4NaOH+O2反应中,每消耗lmol Na2O2生成16g O2;
②除去NaCl溶液中少量的Na2SO4杂质,要判断所加BaCl2溶液是否过量,可向滤液中加入X溶液.X可以是D(填代号)
A.NaOH B.AgNO3 C.HCI D.Na2SO4
(3)配平下面化学方程式,回答下列问题:
3C+K2Cr2O7+8H2SO4=2K2SO4+3CO2↑+2Cr2(SO4)3+8H2O
①H2SO4在上述反应中表现出来的性质是(填选项编号)C.
A.氧化性. B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为4.48L.
(4)在一个密闭容器中放人M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,按要求回答下列问题:
该变化的基本反应类型是分解反应,Q物质的作用为催化剂.
(1)下列是某同学对有关物质进行分类的列表:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | SO3 |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
(2)下列2个反应,按要求填写相关量.
①2Na2O2+2H2O=4NaOH+O2反应中,每消耗lmol Na2O2生成16g O2;
②除去NaCl溶液中少量的Na2SO4杂质,要判断所加BaCl2溶液是否过量,可向滤液中加入X溶液.X可以是D(填代号)
A.NaOH B.AgNO3 C.HCI D.Na2SO4
(3)配平下面化学方程式,回答下列问题:
3C+K2Cr2O7+8H2SO4=2K2SO4+3CO2↑+2Cr2(SO4)3+8H2O
①H2SO4在上述反应中表现出来的性质是(填选项编号)C.
A.氧化性. B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为4.48L.
(4)在一个密闭容器中放人M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,按要求回答下列问题:
| 物质 | M | N | Q | P |
| 反应前质量(g) | 50 | 1 | 3 | 12 |
| 反应后质量(g) | X | 26 | 3 | 30 |
2.下列离子方程式正确的是( )
| A. | 钠与水反应 Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钠与稀硫酸反应CO32-+2H+═CO2↑+H2O | |
| C. | 氢氧化铜与稀硫酸反应OH-+H+═H2O | |
| D. | 铁与盐酸反应2Fe+6H+═2Fe3++3H2↑ |
19.只用水不能鉴别的一组物质是( )
| A. | 乙醇和乙酸 | B. | 乙酸乙酯和乙醇 | C. | 苯和四氯化碳 | D. | 苯和乙酸 |

 ,A的晶体类型离子晶体.
,A的晶体类型离子晶体.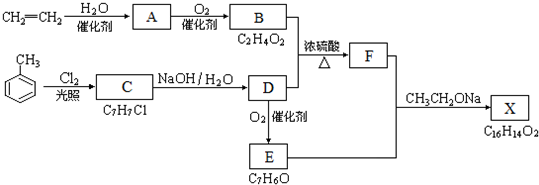
 ;
; ;
;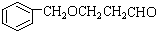 B、
B、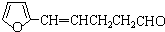
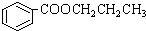
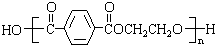 ,其合成单体为
,其合成单体为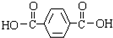 和HOCH2CH2OH;
和HOCH2CH2OH;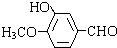 )的重要原料,写出同时满足下列条件的M的同分异构体的结构简式:
)的重要原料,写出同时满足下列条件的M的同分异构体的结构简式: .
.