题目内容
下列说法中正确的是( )
| A、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降 |
| B、常温下,c(NH4+)相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
| C、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D、当溶液中存在的离子只有Cl-、OH-、NH4+、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
考点:离子浓度大小的比较
专题:
分析:A.氨水稀释后溶液中氢氧根离子、铵根离子浓度减小,由于水的离子积不变,则氢离子浓度增大;
B.根据化学式组成及铵根离子水解程度较小可知,浓度相等时③NH4Cl中铵根离子浓度最小,然后根据亚铁离子抑制了铵根离子水解、碳酸根离子水解促进了铵根离子判断等浓度的四种溶液中铵根离子浓度大小,然后判断铵根离子浓度相等时四种溶液的浓度大小;
C.碳酸氢钠溶液显示碱性,则碳酸氢根离子的水解程度大于其电离程度,c(CO32-)<c(H2CO3);
D.根据电荷守恒判断,c(Cl-)>c(NH4+)>c(OH-)>c(H+)中总负电荷大于正电荷,违反了电荷守恒.
B.根据化学式组成及铵根离子水解程度较小可知,浓度相等时③NH4Cl中铵根离子浓度最小,然后根据亚铁离子抑制了铵根离子水解、碳酸根离子水解促进了铵根离子判断等浓度的四种溶液中铵根离子浓度大小,然后判断铵根离子浓度相等时四种溶液的浓度大小;
C.碳酸氢钠溶液显示碱性,则碳酸氢根离子的水解程度大于其电离程度,c(CO32-)<c(H2CO3);
D.根据电荷守恒判断,c(Cl-)>c(NH4+)>c(OH-)>c(H+)中总负电荷大于正电荷,违反了电荷守恒.
解答:
解:A.稀释0.1mol/L的氨水,c(OH-)、c(NH4+)减小,而温度不变,水的离子积不变,则c(H+)升高,故A错误;
B.等浓度的①(NH4)2SO4 ②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3中,由于铵根离子水解程度较小,则③NH4Cl的c(NH4+)最小,②中亚铁离子抑制了铵根离子水解,则②中铵根离子浓度最大,四种溶液的浓度相等时c(NH4+)的关系为:②>①>④>③,则c(NH4+)相同时,物质的量浓度大小关系是:②<①<④<③,故B正确;
C.pH=8.3的NaHCO3溶液中,碳酸氢根离子的水解程度大于其电离程度,则:c(CO32-)<c(H2CO3),溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(H2CO3),>c(CO32-),故C错误;
D.溶液中一定满足电荷守恒,而c(Cl-)>c(NH4+)>c(OH-)>c(H+)中阴离子所带负电荷大于阳离子所带正电荷,不满足电荷守恒,故D错误;
故选B.
B.等浓度的①(NH4)2SO4 ②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3中,由于铵根离子水解程度较小,则③NH4Cl的c(NH4+)最小,②中亚铁离子抑制了铵根离子水解,则②中铵根离子浓度最大,四种溶液的浓度相等时c(NH4+)的关系为:②>①>④>③,则c(NH4+)相同时,物质的量浓度大小关系是:②<①<④<③,故B正确;
C.pH=8.3的NaHCO3溶液中,碳酸氢根离子的水解程度大于其电离程度,则:c(CO32-)<c(H2CO3),溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(H2CO3),>c(CO32-),故C错误;
D.溶液中一定满足电荷守恒,而c(Cl-)>c(NH4+)>c(OH-)>c(H+)中阴离子所带负电荷大于阳离子所带正电荷,不满足电荷守恒,故D错误;
故选B.
点评:本题考查了溶液中离子浓度大小比较,题目难度中等,注意掌握盐的水解原理及其影响,能够根据电荷守恒、物料守恒、质子守恒、盐的水解的影响等知识判断溶液中离子浓度大小,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
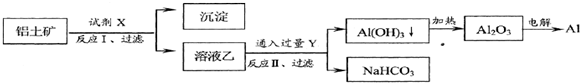
对上述流程中的判断正确的是( )

对上述流程中的判断正确的是( )
| A、试剂X为稀硫酸 |
| B、结合质子( H+)的能力由强到弱的顺序是:AlO2->OH->CO32- |
| C、反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
| D、Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al |
一定能在下列溶液中大量共存的离子组是( )
| A、c(H+)=1×10-2mol?L-1的溶液:Na+、NH4+、CO32-、SO42- |
| B、水电离产生的c(H+)=1×10-12mol/L溶液:Fe2+、Ca2+、I-、NO3- |
| C、含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| D、能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32- |
Fe2O3、ZnO、CuO的固体混合粉末ag,在加热条件下用足量CO还原,得到金属混合物2.39g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5g白色沉淀,则a的数值为( )
| A、3.41 | B、3.21 |
| C、3.19 | D、3.59 |