题目内容
4.铬是一种具有银白色光泽的金属,无毒,化学性质很稳定,工业上以铬铁矿(主要成分是Fe(CrO2)2)为原料冶炼铬及获得强氧化剂Na2Cr2O3,其工艺流程如图1所示(1)写出高温氧化时,生成Na2CrO4的化学反应方程式4Fe(CrO2)2+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2
(2)Cr(OH)2和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)2溶于氢氧化钠溶液的离子方程式Cr(OH)3+OH-=CrO2-+2H2O
(3)酸化过程中,不选用盐酸的原因是氯离子具有还原性,易被氧化为氯气
(4)固体a的主要成分是Na2SO4•10H2O.根据如图2分析操作a为蒸发浓缩、冷却结晶过滤.
(5)加入Na2S溶液反应后,硫元素全部以S2O32-的形式存在.写出S2O32-的离子方程式6S2-+8CrO42-+23H2O=3S2O32-+8Cr(OH)3+22OH-
(6)写出利用铝热反应制取铬的化学方程式2Al+Cr2O3$\frac{\underline{\;高温\;}}{\;}$2Cr+Al2O3.
(7)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol•L-1以下才能排放.可采用加入可溶性钡盐生成BaCrO4沉淀,[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸处理多余的Ba2+的方法处理废水,加入可溶性钡盐后,废水中Ba2+的浓度应不小于2.4×10-4mol•L-1,废水处理后方能达到国家排放标准.
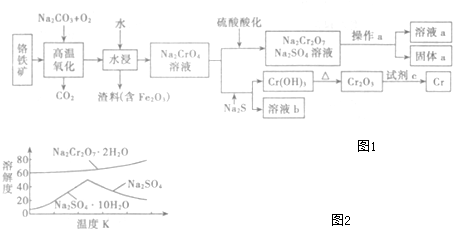
分析 铬铁矿(主要成分是Fe(CrO2)2)为原料冶炼铬及获得强氧化剂Na2Cr2O3,流程分析铬铁矿加入碳酸钠和氧气高温氧化生成Na2CrO4,二氧化碳和氧化铁,水浸过滤得到渣料氧化铁和滤液Na2CrO4溶液,溶液中加入稀硫酸酸化生成重铬酸钠和硫酸钠溶液,通过蒸发浓缩冷却结晶,依据溶解度图象分析可知,过滤得到固体a的主要成分是Na2SO4•10H2O,溶液a为重铬酸钾溶液,另一份Na2CrO4溶液中加入Na2S发生氧化还原反应,硫元素全部以S2O32-的形式存在.铬元素生成氢氧化铬沉淀,过滤后灼烧得到氧化铬,利用铝热反应制备金属铬;
(1)高温氧化时,Fe(CrO2)2和碳酸钠、氧气反应氧化还原反应生成Na2CrO4,二氧化碳和氧化铁,依据原子守恒配平书写化学方程式;
(2)Cr(OH)3溶于氢氧化钠溶液生成CrO2-;
(3)酸化过程中,不选用盐酸的原因是氯离子具有还原性易被氧化为氯气;
(4)与溶解度图象分析,得到硫酸钠晶体的方法是利用重铬酸钠溶解度随温度变化不大,硫酸钠溶解度速温度变化大,可以利用蒸发浓缩,冷却结晶,过滤得到晶体;
(5)加入Na2S溶液反应后,和Na2CrO4溶液反应生成氢氧化铬,硫元素全部以S2O32-的形式存在,依据原子守恒书写离子方程式;
(6)氧化铬和铝高温反应生成铬和氧化铝;
(7)依据饱和溶液中铬酸钡的溶度积计算得到.
解答 解:铬铁矿(主要成分是Fe(CrO2)2)为原料冶炼铬及获得强氧化剂Na2Cr2O3,流程分析铬铁矿加入碳酸钠和氧气高温氧化生成Na2CrO4,二氧化碳和氧化铁,水浸过滤得到渣料氧化铁和滤液Na2CrO4溶液,溶液中加入稀硫酸酸化生成重铬酸钠和硫酸钠溶液,通过蒸发浓缩冷却结晶,依据溶解度图象分析可知,过滤得到固体a的主要成分是Na2SO4•10H2O,溶液a为重铬酸钾溶液,另一份Na2CrO4溶液中加入Na2S发生氧化还原反应,硫元素全部以S2O32-的形式存在.铬元素生成氢氧化铬沉淀,过滤后灼烧得到氧化铬,利用铝热反应制备金属铬;
(1)高温氧化时,Fe(CrO2)2和碳酸钠、氧气反应氧化还原反应生成Na2CrO4,二氧化碳和氧化铁,依据原子守恒配平书写化学方程式,4Fe(CrO2)2+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2,故答案为:4Fe(CrO2)2+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2;
(2)Cr(OH)3溶于氢氧化钠溶液生成CrO2-,反应的离子方程式为:Cr(OH)3+OH-=CrO2-+2H2O,故答案为:Cr(OH)3+OH-=CrO2-+2H2O;
(3)酸化过程中,不选用盐酸的原因:是氯离子具有还原性,易被氧化为氯气,故答案为:氯离子具有还原性,易被氧化为氯气;
(4)结合溶解度图象分析,溶液中得到硫酸钠晶体的方法是:利用重铬酸钠溶解度随温度变化不大,硫酸钠溶解度速温度变化大,可以利用蒸发浓缩,冷却结晶,过滤得到晶体,故答案为:蒸发浓缩;冷却结晶;
(5)加入Na2S溶液反应后,和Na2CrO4溶液反应生成氢氧化铬,硫元素全部以S2O32-的形式存在,依据原子守恒书写离子方程式为,6S2-+8CrO42-+23H2O=3S2O32-+8Cr(OH)3+22OH-,故答案为:6S2-+8CrO42-+23H2O=3S2O32-+8Cr(OH)3+22OH-;
(6)氧化铬和铝高温反应生成铬和氧化铝,反应的化学方程式为:2Al+Cr2O3$\frac{\underline{\;高温\;}}{\;}$2Cr+Al2O3,故答案为:2Al+Cr2O3$\frac{\underline{\;高温\;}}{\;}$2Cr+Al2O3 ;
(7)依据饱和溶液中铬酸钡的溶度积计算得到,Ksp(BaCrO4)=1.2×10-10,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol•L-1以下才能排放,则废水中Ba2+的浓度应不小于c(Ba2+)=$\frac{Ksp}{c(Cr{{O}_{4}}^{2-})}$=$\frac{1.2×1{0}^{-10}}{5.0×1{0}^{-7}}$=2.4×10-4mol/L,故答案为:2.4×10-4mol/L.
点评 本题考查了物质分离提纯的方法和过程分析判断,主要是物质溶解性、氧化还原反应产物的分析应用,离子方程式书写方法,溶度积计算等,掌握分析流程的方法和基础知识是关键,题目难度中等.

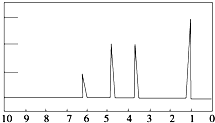 1H核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为δ)也就不同.现有一物质的1H核磁共振谱如图所示:则该物质可能是下列中的( )
1H核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为δ)也就不同.现有一物质的1H核磁共振谱如图所示:则该物质可能是下列中的( )| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | CH3CH2CH2CH3 | D. | CH3CH2OH |
| A. | 12.5g | B. | 13.2g | C. | 19.7g | D. | 24.4g |
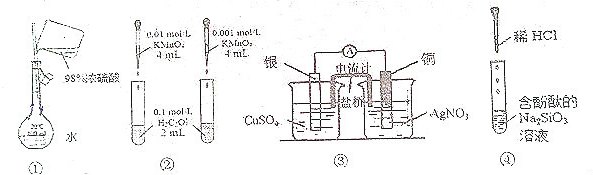
| A. | 装置①配制一定的物质的量浓度的稀硫酸溶液 | |
| B. | 装置②根据溶液褪色的快慢比较浓度对反应速率的影响 | |
| C. | 装置③制作原电池 | |
| D. | 装置④制备硅胶 |
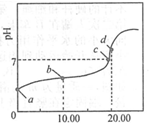 常温下,用0.01mol•L-1NaOH溶液滴定20.00mL0.01mol•L-1CH3COOH溶液,所得滴定曲线如图.下列说法正确的是( )
常温下,用0.01mol•L-1NaOH溶液滴定20.00mL0.01mol•L-1CH3COOH溶液,所得滴定曲线如图.下列说法正确的是( )| A. | a点PH=2 | |
| B. | b点对应的溶液中:c(OH-)+c(CH3COO-)=c(Na+)+c(H+) | |
| C. | c点表示NaOH溶液与CH3COOH溶液恰好完全反应 | |
| D. | d点对用的溶液中,水的电离程度小于同温下纯水的电离程度 |
| A. | 该反应的正反应为放热反应 | |
| B. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 反应的热化学方程式可表示为:CO(g)+H2O(g)$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO2(g)+H2(g)△H<0 kJ/mol |

| 选项 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 还原性:I->Br+>Cl- |
| C | 开始铜粉不溶解,溶液呈无色,后有气体放出,溶液呈蓝色 | 氧化性:NaNO3>H2SO4>Cu2+ |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
| A. | pH=1的溶液中:Na+、Cl-、K+、HS- | |
| B. | 水电离出的c(H+)=10-12mol/L中:Ba2+、K+、Cl-、CO32- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的水溶液中:CH3COO-、CO32-、Na+、K+ | |
| D. | c(Al3+)=1mol/L的溶液中:Na+、NO3-、SO42-、HCO3- |