题目内容
12.常温下某溶液中,水电离出的[0H-]=10-5mol•L-1,该溶液中的溶质可能是( )| A. | 氯化铵 | B. | 醋酸钠 | C. | 氢氧化钠 | D. | 硫酸氢钠 |
分析 室温下,某溶液中由水电离产生的[0H-]=10-5mol•L-1>10-7 mol/L,说明水的电离受到促进,则溶液中的溶质为能水解的盐,如氯化铵、醋酸钠等溶液,据此分析解答.
解答 解:室温下,某溶液中由水电离产生的[0H-]=10-5mol•L-1>10-7 mol/L,说明溶质促进了水的电离,
A.NH4Cl溶液中铵根离子水解,促进了水的电离,故A正确;
B.醋酸钠溶液中,醋酸根离子水解促进了水的电离,故B正确;
C.Ba(OH)2属于强碱而抑制水电离,故C错误;
D.NaHSO4属于强酸酸式盐,完全电离出的氢离子抑制水的电离,故D错误;
故选AB.
点评 本题了水的电离及其影响,题目难度不大,侧重考查学生的分析能力,明确物质的性质是解本题关键,注意掌握酸碱溶液及能够水解的盐溶液对水的电离的影响.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
2.下列物质不可以导电的是( )
| A. | 蔗糖 | B. | Cu | C. | NaCl溶液 | D. | HCl溶液 |
20.ag铁粉与一定质量的硝酸溶液充分反应后,铁完全溶解,生成的气体下bL氧气混合后,恰好能被水完全吸收,a和b的关系不可能为( )
| A. | b=0.2a | B. | b=0.3a | C. | b=0.25a | D. | a=2b |
7.把下列四种物质分别加入到盛有100mL盐酸的烧杯中,能使盐酸导电性发生明显变化的是( )
| A. | 10g NaCl | B. | 10g NaOH固体 | C. | 10g BaSO4固体 | D. | 10g AgNO3固体 |
20.下列化学用语正确的是( )
| A. | HCO3-+H2O═CO32-+H3O+ | B. | NaCl(S)═Na+(aq)+Cl-(aq) | ||
| C. | S2-+H2O?H2S+2OH- | D. | SiO32-+H2O?H2SiO3+2OH- |
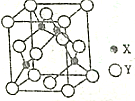 已知常见元素X的原子序数比常见元素Y的小,X的氢化物能与其最高价氧化物的水化物发生化合反应生成一种离子化合物M,Y元素的周期序数等于最外层电子数.回答下列问题:
已知常见元素X的原子序数比常见元素Y的小,X的氢化物能与其最高价氧化物的水化物发生化合反应生成一种离子化合物M,Y元素的周期序数等于最外层电子数.回答下列问题: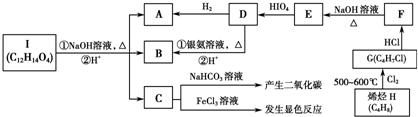
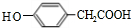 ,E
,E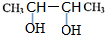 ;
; ;
;