题目内容
16.因发现青蒿素、开创治疗疟疾新方法,中国药学家屠呦呦获得2015年获诺贝尔生理学或医学奖.青蒿素的分子式为C15H22O5,不能发生酯化反应,在热的酸、碱溶液中不能稳定存在.下列结构简式中有一种是青蒿素的结构简式.由此判断青蒿素的结构简式为( )| A. | 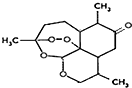 | B. | 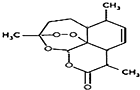 | ||
| C. | 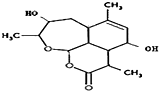 | D. | 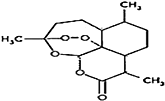 |
分析 青蒿素的分子式为C15H22O5,不能发生酯化反应说明不含羟基和羧基,在热的酸、碱溶液中不能稳定存在说明分子中含有酯键,酸碱条件下发生水解反应,依据所具有官能团存在判断结构简式.
解答 解:A.分子中无羧基和羟基,不能发生酯化反应,无酯键在热的酸、碱溶液中能稳定存在,故A错误;
B.存在酯键,在热的酸、碱溶液中不能稳定存在,无羧基和醇羟基不能发生酯化反应,故B错误;
C.分子中含有酯键,在热的酸、碱溶液中不能稳定存在,含羟基能发生酯化反应,故C错误;
D.分子中含酯键,在热的酸、碱溶液中不能稳定存在,无羧基和羟基,不能发生酯化反应,故D正确;
故选D.
点评 本题考查了有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酯、醇、酸的性质,题目难度不大.

练习册系列答案
相关题目
7.一定条件下,在容积为5L密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),半分钟后测得生成0.04molSO3.在这段时间内O2的化学反应速率为( )
| A. | 0.004(mol•L-1•min-1) | B. | 0.008(mol•L-1•min-1) | ||
| C. | 0.016(mol•L-1•min-1) | D. | 0.032(mol•L-1•min-1) |
4.A、B两种有机物组成的混合物,当混合物质量相等时,无论A、B以何种比例混合,完全燃烧产生二氧化碳的量均相等,符合这一组合的条件有:①同分异构体;②同系物;③具有相同的最简式;④含碳的质量分数相同,其中正确的是( )
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
11.碱性镍锌(NiZn)电池是一种可以替代镍氢电池的新型电池,其总反应为:2NiOOH+2H2O+Zn$?_{充电}^{放电}$2Ni(OH)2+Zn(OH)2.则下列说法中错误的是( )
| A. | 电池工作时,OH-向负极移动 | |
| B. | 放电时负极反应式:Zn-2e-+2OH-═Zn(OH)2 | |
| C. | 充电时,与外电源正极相连的电极上电极反应式为Ni(OH)2-e-+OH-═NiOOH+H2O | |
| D. | 该电池电解1L 0.3 mol/LAgNO3溶液,若产生1.12L气体(标准状况),溶液pH变为2 |
1.亚碳化合物的特征是在1个碳原子上带有2个未成对电子,亚碳化合物是具有很高反应活性的有机化合物.下列属于亚碳化合物的是( )
| A. | CH3 | B. | H2C5(线状) | C. | 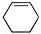 | D. | CH2═CH2 |
8.苯乙酸的同分异构体中属于芳香酯类的有( )种.
| A. | 6 | B. | 5 | C. | 4 | D. | 7 |
5.下列关于化学用语的表示正确的是( )
| A. | 中子数为20的氯(Cl)原子: | B. | CO2的电子式: | ||
| C. | CCl4分子的比例模型: | D. | 镁的离子结构示意图: |
 ,B为18电子分子,其结构式为
,B为18电子分子,其结构式为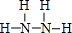 .
. .
. .
. 形成六元环酯的产物的结构简式
形成六元环酯的产物的结构简式 .
.