��Ŀ����
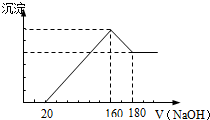 ��һ��������þ���Ͻ�Ͷ��100mLһ��Ũ�ȵ������У��Ͻ���ȫ�ܽ⣮�������� Һ�еμ�Ũ��Ϊ5mol/L��NaOH��Һ�����ɵij����������NaOH��Һ�������ϵ��ͼ���������������λ��mL��������������λ��g����Ӧ�������漰�Ļ�ѧ����ʽ
��һ��������þ���Ͻ�Ͷ��100mLһ��Ũ�ȵ������У��Ͻ���ȫ�ܽ⣮�������� Һ�еμ�Ũ��Ϊ5mol/L��NaOH��Һ�����ɵij����������NaOH��Һ�������ϵ��ͼ���������������λ��mL��������������λ��g����Ӧ�������漰�Ļ�ѧ����ʽ�У���6HCl+2Al�T2AlCl3+3H2��
��2HCl+Mg�TMgCl2+H2��
��HCl+NaOH�TNaCl+H2O
��2NaOH+MgCl2�TMg��OH��2��+2NaCl
��Al��OH��3+NaOH�TNaAlO2+2H2O
��3NaOH+AlCl3�TAl��OH��3��+3NaCl
��1������NaOH��Һ0--20mL�����з�Ӧ����ʽΪ��
��2���Ͻ���Al������Ϊ
���㣺�йػ���ﷴӦ�ļ���,���ӷ���ʽ���йؼ���
ר�⣺������
��������1����ͼ��֪���ӿ�ʼ������NaOH��Һ20mL��û�г������ɣ�˵��ԭ��Һ�������ܽ�Mg��Al��������ʣ�࣬��ʱ�����ķ�ӦΪ��HCl+NaOH=NaCl+H2O��
�����μ�NaOH��Һ��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ���ټ����μ�NaOH��Һ�������������������Ʒ�Ӧ����ƫ��������ˮ��������ӦAl��OH��3+NaOH=NaAlO2+2H2O��
��2����ͼ��֪���Ӽ���20m����������ҺL��ʼ������������������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=��0.16L-0.02L����5mol/L=0.7mol���Ӽ�������������Һ160mL��180mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O������n[Al��OH��3]=��0.18L-0.16L����5mol/L=0.1mol��������m=nM����Al��������
��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH�����ݴ˼����n��HCl����������c=
������������ʵ���Ũ�ȣ�
�����μ�NaOH��Һ��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ���ټ����μ�NaOH��Һ�������������������Ʒ�Ӧ����ƫ��������ˮ��������ӦAl��OH��3+NaOH=NaAlO2+2H2O��
��2����ͼ��֪���Ӽ���20m����������ҺL��ʼ������������������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=��0.16L-0.02L����5mol/L=0.7mol���Ӽ�������������Һ160mL��180mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O������n[Al��OH��3]=��0.18L-0.16L����5mol/L=0.1mol��������m=nM����Al��������
��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH�����ݴ˼����n��HCl����������c=
| n |
| V |
���
�⣺��1����ͼ��֪���ӿ�ʼ������NaOH��Һ20mL��û�г������ɣ�˵��ԭ��Һ�������ܽ�Mg��Al��������ʣ�࣬��ʱ�����ķ�ӦΪ��HCl+NaOH=NaCl+H2O��
�����μ�NaOH��Һ��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ���ټ����μ�NaOH��Һ�������������������Ʒ�Ӧ����ƫ��������ˮ��������ӦAl��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��HCl+NaOH=NaCl+H2O��Al��OH��3+NaOH=NaAlO2+2H2O��
��2����ͼ��֪���Ӽ���20m����������ҺL��ʼ������������������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪��3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=��0.16L-0.02L����5mol/L=0.7mol��
�Ӽ�������������Һ160mL��180mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O��
����n[Al��OH��3]=��0.18L-0.16L����5mol/L=0.1mol�����������غ��֪��m��Al��=27g/mol��0.1mol=2.7g��
��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH��=0.16L��5mol/L=0.8mol��������Ԫ���غ�n��HCl��=0.8mol��
����������ʵ���Ũ��Ϊ��
=8mol/L��
�ʴ�Ϊ��2.7��8��
�����μ�NaOH��Һ��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ���ټ����μ�NaOH��Һ�������������������Ʒ�Ӧ����ƫ��������ˮ��������ӦAl��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��HCl+NaOH=NaCl+H2O��Al��OH��3+NaOH=NaAlO2+2H2O��
��2����ͼ��֪���Ӽ���20m����������ҺL��ʼ������������������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪��3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=��0.16L-0.02L����5mol/L=0.7mol��
�Ӽ�������������Һ160mL��180mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O��
����n[Al��OH��3]=��0.18L-0.16L����5mol/L=0.1mol�����������غ��֪��m��Al��=27g/mol��0.1mol=2.7g��
��������������ҺΪ160mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH��=0.16L��5mol/L=0.8mol��������Ԫ���غ�n��HCl��=0.8mol��
����������ʵ���Ũ��Ϊ��
| 0.8mol |
| 0.1L |
�ʴ�Ϊ��2.7��8��
���������⿼��þ�����������ʡ������ļ��㣬��Ŀ�Ѷ��еȣ���ͼ�������ʽ���飬�����������Ѷȣ�����ͼ����εķ����ķ�Ӧ�ǽ���ؼ����������غ�˼����㣮

��ϰ��ϵ�д�
 ����Ӣ��ϵ�д�
����Ӣ��ϵ�д�
�����Ŀ
ij�����廯����A�ķ���ʽΪC8H10O�����Ľṹ������������-CH3����������FeCl3��Һ�ɷ�����ɫ��Ӧ�������Ľṹ���У�������
| A��4�� | B��5�� | C��6�� | D��7�� |
ij��������FeCl3��Һ��ʴ����ͭ�ľ�Ե��������·�壬һʵ��С��Ըó�������·�����õķ�Һ���з�����ȡ50.0 mL��Һ�������м���0.64 g Cu������ͭȫ���ܽ⣮��ȡ50.0 mL��Һ�������м���������AgNO3����������43.05 g������˵����ȷ���ǣ�������
| A��ԭ��Һ�к��еĽ���������ֻ��Fe2+��Cu2+ |
| B���ù���ԭ��ʹ�õ�FeCl3��Һ�����ʵ���Ũ��ԼΪ2 mol/L |
| C������500 mL��Һ�м���������ϡHNO3��Һ���ڱ���²���NO����4.48 L����ԭ��Һ��Fe2+��Cu2+�����ʵ���Ũ��֮��Ϊ2��1 |
| D������ʹ�����軯����Һ����÷�Һ���Ƿ���Fe2+ |
 ������CO��SO2�̵�����Ⱦ��һ�ַ������ǽ����ڴ���������ת��Ϊ����S��g����������ӦΪ��2CO��g��+SO2��g��?S��g��+2CO2��g��
������CO��SO2�̵�����Ⱦ��һ�ַ������ǽ����ڴ���������ת��Ϊ����S��g����������ӦΪ��2CO��g��+SO2��g��?S��g��+2CO2��g��
 ij��ѧ��ȤС����̽����������ת��ʱ�����ֲ������ʴ�����ͼ��ʾ������ת����ϵ�����ַ�Ӧ�������������ȥ����
ij��ѧ��ȤС����̽����������ת��ʱ�����ֲ������ʴ�����ͼ��ʾ������ת����ϵ�����ַ�Ӧ�������������ȥ����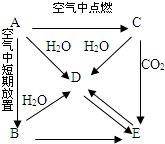 ��A��B��C��D��E�������ʶ���ͬһ��Ԫ�أ�CΪһ�ֵ���ɫ�Ĺ��壮���ǰ���ͼ��ʾ�Ĺ�ϵ�ת������֪AΪ���ʣ���Ҫ��ش����⣮
��A��B��C��D��E�������ʶ���ͬһ��Ԫ�أ�CΪһ�ֵ���ɫ�Ĺ��壮���ǰ���ͼ��ʾ�Ĺ�ϵ�ת������֪AΪ���ʣ���Ҫ��ش����⣮