题目内容
5.下列说法错误的是( )| A. | 84g NaHCO3 溶于1L水配得1mol•L-1 NaHCO3 溶液 | |
| B. | 在标准状况下,44.8L HCl溶于1L水配成2mol•L-1 的盐酸溶液 | |
| C. | 在标准状况下,22.4L NH3溶于水配成1L溶液,浓度为1mol•L-1 | |
| D. | 1mol•L-1 的CaCl2溶液溶液1L,取出100mL,含0.2mol Cl- |
分析 A、溶液的体积不等于溶剂的体积;
B、44.8L HCl溶于1L水后,溶液的体积大于1L;
C、求出氨气的物质的量,然后根据溶液的体积为1L来计算浓度;
D、1mol•L-1 的CaCl2溶液溶液1L,取出100mL时溶液的浓度不变.
解答 解:A、84g NaHCO3 的物质的量为1mol,将其溶于1L水后所得溶液的体积大于1L,则所配制的溶液的浓度小于1mol/L,故A错误;
B、标况下,44.8L HCl的物质的量为2mol,将其溶于1L水后,溶液的体积大于1L,故则所配制的溶液的浓度小于2mol/L,故B错误;
C、在标准状况下,22.4L 氨气的物质的量为1mol,溶于水配成1L的溶液,即溶液的体积为1L,则所得溶液的物质的量浓度C=$\frac{n}{V}$=$\frac{1mol}{1L}$=1mol/L,故C正确;
D、1mol•L-1 的CaCl2溶液溶液1L,取出的100mL溶液的浓度不变仍为1mol/L,故所取出的溶液中的CaCl2的物质的量n=CV=1mol/L×0.1L=0.1mol,含0.2molCl-,即0.2NA个,故D正确.
故选AB.
点评 本题考查了一定物质的量浓度溶液的配制,应注意的是溶液的体积不等于溶剂的体积,难度不大.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 在一定条件下,使煤和氢气作用,可以得到液体燃料,也可以获得洁净的燃料油 | |
| B. | (CH3)2CHCH(CH3)2的系统命名为:2,3-二甲基丁烷 | |
| C. | 硬脂酸甘油酯可以在稀硫酸中水解,也可以在NaOH溶液中发生皂化反应彻底水解 | |
| D. | 氨基酸分子中均含有氨基和羧基,加入浓的硫酸钠溶液可从溶液中析出 |
13.木糖醇是一种新型的甜味剂,是一种理想的蔗糖代替品,它具有甜味适中,溶解性好,适合糖尿病患者等优点,结构简式为:CH2OH(CHOH)3CH2OH.下列有关木糖醇的叙述正确的是( )
| A. | 木糖醇与核糖(C3H10O3)互为同分异构体 | |
| B. | 木糖醇与甘油(CH2OHCHOHCH2OH)互为同系物 | |
| C. | 木糖醇可以与乙酸发生酯化反应 | |
| D. | 木糖醇与葡萄一样是一种单糖 |
20.下列说法正确的是( )
| A. | 有机物就是仅有碳、氢两种元素组成的化合物 | |
| B. | 有机物都是非电解质,不能导电 | |
| C. | 组成符合CnHn的有机物分子一定互为同系物 | |
| D. | 含有醛基(-CHO)的有机物不一定是醛 |
11.一定温度下,固定容器的密闭容器中进行的可逆反应:A(g)+B(g)═C(g)+D(g),当下列物理量不再改变时,表明反应已达到平衡的是( )
| A. | 单位时间内有1mol A生成,有1molC消耗 | |
| B. | 混合气体的密度不变 | |
| C. | A的消耗速率与D的消耗速率相同 | |
| D. | B物质的相对分子质量不变 |
8.某单烯烃与H2加成后的产物是: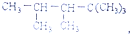 ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )
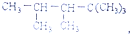 ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 2种 |
9.下列与有机物的结构、性质有关的叙述不正确的是( )
| A. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| B. | C5H12有3种同分异构体 | |
| C. | 氨基酸、淀粉均属于高分子化合物 | |
| D. | 碳原子之间只以单键相结合的链烃为烷烃 |