题目内容
15.已知:2C(s)+O2(g)═2CO(g),△H=-220.6kJ•mol-1
2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ•mol-1
C(s)+H2O(g)═CO(g)+H2(g),△H=akJ•mol-1
则 a 为( )
| A. | ?263 | B. | +263 | C. | ?352.1 | D. | +131.5 |
分析 已知:①2C(s)+O2(g)═2CO(g),△H=-220.6kJ•mol-1②2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ•mol-1,可利用盖斯定律,将$\frac{①-②}{2}$得到C(s)+H2O(g)═CO(g)+H2(g)的反应热,以此解答该题.
解答 解:已知:①2C(s)+O2(g)═2CO(g),△H=-220.6kJ•mol-1②2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ•mol-1,可利用盖斯定律,将$\frac{①-②}{2}$得到C(s)+H2O(g)═CO(g)+H2(g)△H=$\frac{(-220.6kJ/mol)-(-483.6kJ/mol)}{2}$=+131.5kJ/mol,
故选D.
点评 本题考查化学反应与能量变化,为高频考点,侧重考查学生的分析、计算能力,注意把握盖斯定律的运用,难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
20.向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
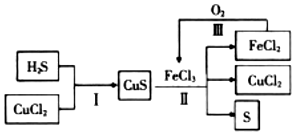

| A. | 在转化过程中化合价不变的元素只有Cu和Cl | |
| B. | 反应II中每生成1.25molS需要2.5molFeCl3 | |
| C. | 在转化过程中能循环利用的物质有FeCl2和CuCl2 | |
| D. | 反应Ⅲ中消耗1molO2时,可转化4mol的FeCl2 |
7.一定温度下,向2L恒容容器中充入1molA和1molB,发生反应A(g)+B(g)=C(g)经过一段时间后达到平衡,反应过程中测定的部分数据如表.下对说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 | ||
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 | ||
| A. | 前 5 s 的平均反应速率v(A)=0.03 mol•L-1•s-1 | |
| B. | 正反应是吸热反应 | |
| C. | 保持温度不变,起始时向容器中充入2molC,达平衡时,C的转化率大于80% | |
| D. | 保持温度不变,起始时向容器中充入0.2molA、0.2molB?和1molC,反应达到平衡前v(正)<v(逆) |
4.下列由实验现象推出的结论正确的是( )
| A. | 向某溶液中加入CCl4,CCl4层显紫色,说明原溶液中存在I- | |
| B. | 某溶液中滴加NaOH生成白色沉淀,迅速变成灰绿色,最终变成红褐色,则原溶液有Fe2+,无Fe3+ | |
| C. | 将CO2通入某溶液中,不能产生白色沉淀,说明原溶液中不含Ba2+或Ca2+ | |
| D. | 用干净的铂丝蘸取某溶液在酒精灯外焰上灼烧,火焰呈黄色,说明该溶液中有Na+无K+ |