题目内容
10.铁是人类较早使用的金属之一,运用铁及其化合物的知识,完成下列问题.(1)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:2Fe3++Cu=2Fe2++Cu2+.某问学对FeCl3腐蚀铜后所得溶液的组成进行测定:取少最待侧溶液,滴入KSCN 溶液后显红色.由此可知,该溶液中所含金属阳离子有Fe3+、Fe2+、Cu2+.
(2)欲从废液中回收铜,并重新获得FeCl3溶液.某同学设计如下实验方案:
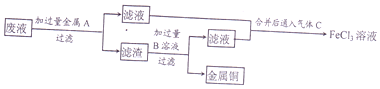
①写出上述实验中有关物质的化学式:AFe;BHCl.
②写出通入气体C的化学方程式:2FeCl2+Cl2=2FeCl3.
分析 (1)氯化铁与铜反应生成氯化亚铁与氯化铜;取少量待测溶液,滴入KSCN溶液呈红色,则一定含铁离子;
(2)腐蚀废液中含有氯化铜、氯化亚铁,加入过量的铁可以和氯化铜反应生成金属铜和氯化亚铁,故A为Fe,经过滤所得滤液是氯化亚铁,滤渣是金属铜和过量的铁,铜不能盐酸反应,而金属铁可以,加入过量B为盐酸可以将铜分离,得到的滤液为氯化亚铁,滤液合并后通入氯气,能将亚铁离子氧化为三价铁,以此解答该题.
解答 解:(1)FeCl3溶液与铜反应生成氯化铜、氯化亚铁,离子反应为2Fe3++Cu=2Fe2++Cu2+;取少量待测溶液,滴入KSCN溶液呈红色,则一定含铁离子,则Cu不足,溶液中还含Fe2+、Cu2+;
故答案为:2Fe3++Cu=2Fe2++Cu2+;Fe3+、Fe2+、Cu2+;
(2)腐蚀废液中含有氯化铜、氯化亚铁,加入过量的铁可以和氯化铜反应生成金属铜和氯化亚铁,故A为Fe,经过滤所得滤液是氯化亚铁,滤渣是金属铜和过量的铁,铜不能盐酸反应,而金属铁可以,加入过量B为盐酸可以将铜分离,得到的滤液为氯化亚铁,滤液合并后通入氯气,能将亚铁离子氧化为三价铁,
①由上述分析可知,A为Fe,B为HCl;
故答案为:Fe;HCl;
②C为氯气,通入C和氯化亚铁反应生成氯化铁,方程式为2FeCl2+Cl2=2FeCl3;
故答案为:2FeCl2+Cl2=2FeCl3.
点评 本题考查了铁及其化合物的性质,涉及的内容较多,注意分析题中提供的信息,根据所学知识写成反应的方程式,注意把握物质的性质及反应原理,综合性较强,题目难度不大.

练习册系列答案
相关题目
20.下列物质中,是人体必需的营养成分之一,给人体提供能量的是( )
| A. | 食盐 | B. | 水 | C. | 糖类 | D. | 陈醋 |
1.用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
| A. | 1 g H2含有的氢原子数目为2NA | |
| B. | 常温常压下,22.4 L O2含有的分子数目为NA | |
| C. | 1 L 1 mol•L-1 KOH溶液中含有的钾离子数目为NA | |
| D. | 1 mol Zn变为Zn2+失去的电子数目为NA |
18.下列说法中,正确的是( )
| A. | 硅元素在自然界里均以化合态存在 | |
| B. | SiO2不能与水反应生成硅酸,不是酸性氧化物 | |
| C. | 除去二氧化硅中少量的碳酸钙杂质应选用水 | |
| D. | 粗硅制备时,发生的反应为C+SiO2=Si+CO2↑ |
15.已知:
2C(s)+O2(g)═2CO(g),△H=-220.6kJ•mol-1
2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ•mol-1
C(s)+H2O(g)═CO(g)+H2(g),△H=akJ•mol-1
则 a 为( )
2C(s)+O2(g)═2CO(g),△H=-220.6kJ•mol-1
2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ•mol-1
C(s)+H2O(g)═CO(g)+H2(g),△H=akJ•mol-1
则 a 为( )
| A. | ?263 | B. | +263 | C. | ?352.1 | D. | +131.5 |
19.当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A. | 泥浆 | B. | Fe(OH)3 胶体 | C. | 酒精 | D. | CuSO4溶液 |
20.在Al3++3H2O≒Al(OH)3+3H+的平衡体系中,要抑制Al3+的水解,可采取的措施为( )
| A. | 加热 | B. | 通入氯化氢气体 | ||
| C. | 加入适量的氢氧化钠溶液 | D. | 加入固体AlCl3 |
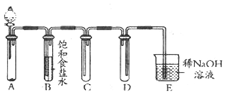 如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.
如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.