题目内容
10.下列离子方程式正确的是( )| A. | Cl2与H2O反应:Cl2+H2O═2H++ClO-+Cl- | |
| B. | 往FeCl3溶液中加入Cu粉:Fe3++Cu═Fe2++Cu2+ | |
| C. | 向AlCl3溶液中滴加氨水至过量:Al3++3OH-═Al(OH)3↓ | |
| D. | 将铜片投入浓硝酸中:2NO3-+Cu+4H+═Cu2++2NO2↑+2H2O |
分析 A.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
B.离子方程式两边正电荷不相等,违反了电荷守恒;
C.氨水为弱碱,离子方程式中一水合氨不能拆开;
D.铜与浓硝酸反应生成硝酸铜、二氧化氮气体和水.
解答 解:A.Cl2与H2O反应生成氯化氢和次氯酸,正确的离子方程式为:Cl2+H2O═H++HClO+Cl-,故A错误;
B.往FeCl3溶液中加入Cu粉,反应生成硫化铜和氯化亚铁,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故B错误;
C.向AlCl3溶液中滴加氨水至过量,一水合氨不能拆开,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.铜片投入浓硝酸中生成二氧化氮气体,反应的离子方程式为:2NO3-+Cu+4H+═Cu2++2NO2↑+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
1.下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)C的离子结构示意图为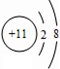 ,I的原子结构示意图
,I的原子结构示意图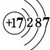 .
.
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为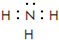 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
(3)元素的最高价氧化物对应的水化物中,碱性最强的是NaOH,该碱化学键类型离子键和共价键,酸性最强的是HClO4,呈两性的是Al(OH)3.
(4)A分别与D、E、F、G H形成的化合物的稳定性顺序为:CH4<NH3<H2O<HF.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | B | ||||||
| 2 | D | E | F | G | ||||
| 3 | C | H | I |
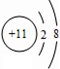 ,I的原子结构示意图
,I的原子结构示意图 .
.(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
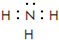 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).(3)元素的最高价氧化物对应的水化物中,碱性最强的是NaOH,该碱化学键类型离子键和共价键,酸性最强的是HClO4,呈两性的是Al(OH)3.
(4)A分别与D、E、F、G H形成的化合物的稳定性顺序为:CH4<NH3<H2O<HF.
5.下列关于元素周期表的说法正确的是( )
| A. | 元素周期表是按照元素相对原子质量大小排列而成的 | |
| B. | 元素周期表有7个横行,也是7个周期;有18个纵行,即18个族 | |
| C. | 凡是位于元素周期表中同一周期的元素,都是按从左到右的顺序原子最外层电子数由1递增到8 | |
| D. | 凡是位于元素周期表中同一主族的元素,都是按从上到下的顺序电子层数逐渐增多 |
19.在某稀溶液中含4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe粉,充分反应(已知NO3-被还原为NO).下列说法正确的是( )
| A. | 所得溶液中C(Fe2+):C(Fe3+)=1:1 | B. | 所得溶液中C(NO3-)=2.75mol/L | ||
| C. | 反应后生成NO的体积为28 L | D. | 所得溶液中溶质只有FeSO4和K2SO4 |
20. 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
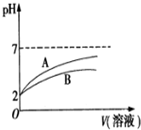
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
①根据表中数据判断t时刻此反应向正反应方向进行(选填“正”或“逆”).
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
| 物质 | Cl2 | TiCl4 | O2 |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
 运用有关知识,回答下列问题.
运用有关知识,回答下列问题.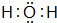 ,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.
,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.
 .
. .
.